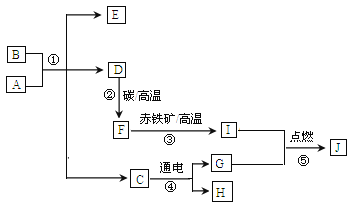
题目内容
【题目】氮化镁(Mg3N2)是一种应用范围非常广泛的化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的化合物,制备特殊的陶瓷材料等。氮化镁是浅黄色粉末,极易与水反应生成氢氧化镁沉淀和氨气,某兴趣小组欲测定某氮化镁样品中氮化镁的质量分数,取氮化镁样品16g按图1装置进行实验,测定氮化镁的纯度,发现B装置增重3.4g。已知Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑(注:B图烧瓶杯底有破洞,瓶中空气与下方液体可接触流通)
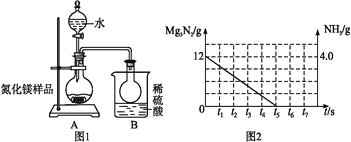
(1)求该样品中氮化镁的质量分数____________(写出计算过程);
(2)导致该样品中氮化镁含量测定结果偏低的可能原因是____________
(3)经过精确测定,知道样品中氮化镁的质量分数为75%,请在图2画出生成的氨气质量的变化曲线。_________________________
【答案】 62.5% 氨气未能全部被吸收等 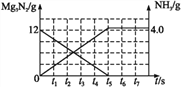
【解析】根据质量守恒定律和题中信息知,生成氨气的质量是3.4g。
解∶设该样品中氮化镁的质量分数是x
Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
100 34
16g×x 3.4g
![]()
![]() =
=![]() ,x= 62.5%。
,x= 62.5%。
(2)导致该样品中氮化镁含量测定结果偏低的可能原因是氨气未能全部被吸收等。
(3)经精确测定,样品中氮化镁的质量分数为75%,在图2画出生成的氨气质量的变化曲线。

点睛∶氮化镁是浅黄色粉末,极易与水反应生成氢氧化镁沉淀和氨气。用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的化合物,制备特殊的陶瓷材料等。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
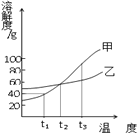
小学生10分钟应用题系列答案【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )

温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A. 乙为NH4Cl
B. t3应介于40℃﹣50℃
C. 55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙
D. 等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等