��Ŀ����
̼������;�dz��㷺���ǹ�ҵ��������Ҫ�Ļ���ԭ�ϣ���1921���ҹ���ѧ����°�����һ�������Ĵ�����������--�������Ƽ����
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ���ڻ�����Ӧ�����е�
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��
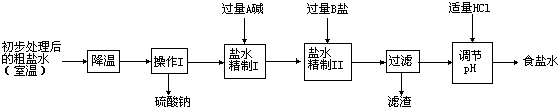
����Ҫ�������£�
��ͨ������ʹ�����ƴӴ���ˮ��������˵�������Ƶ��ܽ�����¶ȵı仯��
�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ��д��������Һ��B���Ƿ������ʵ�鷽����
�ݲ������ϵ�֪NaCl��NH4HCO3��NaHCO3��NH4Cl��30��ʱ���ܽ�����±���ʾ��
| �¶� | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30�� | 41.1g | 27.0g | 11.1g | 36.3g |
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO
| ||
��4���á������Ƽ���ƵõĴ����г������������Ȼ��ƣ�Ϊ�ⶨij������Ʒ��̼���Ƶ�����������С��ͬѧ��ȡ����Ʒ5.6g���뵽ʢ��100g����ϡ������ձ��У���ȫ��Ӧ��Ƶ��ձ��е���Һ����Ϊ103.4g����ô�����Ʒ��̼���Ƶ�����������
��������1�����ݻ��Ϸ�Ӧ�Ķ�����ص�ش�
��2���ٸ��������Ƶ��ܽ�����¶�Ӱ�������ش�
�ڸ��ݼ����ɻش�ǰһ�գ����ݡ�����I���������漰�����������ơ��Ȼ��ơ��Ȼ�þ���������Ƶ����ʻش����ķ�Ӧ��
�۸���̼���ơ��������ƺ��Ȼ��ƵĻ�ѧ���ʼ����ӵ�ԭ��ش�
�ܸ���̼���ƵĻ�ѧ���ʺͼ��鷽���ش�
�ݸ��ݵڶ���ʳ����NH4HCO3��Ӧ�Ǹ��ֽⷴӦ���Լ�̼�����Ƶ��ܽ�Ƚ�С����Ϣ��д����ʽ��
��4�����ⷢ���ķ�ӦΪNa2CO3+2HCl�T2NaCl+CO2��+H2O�����������غ㶨�ɼ������Ӧ���ɵĶ�����̼���������ٸ��ݶ�����̼�������ͻ�ѧ����ʽ���㴿����Ʒ��̼���Ƶ������������ô�����Ʒ��̼���Ƶ�����������
��2���ٸ��������Ƶ��ܽ�����¶�Ӱ�������ش�
�ڸ��ݼ����ɻش�ǰһ�գ����ݡ�����I���������漰�����������ơ��Ȼ��ơ��Ȼ�þ���������Ƶ����ʻش����ķ�Ӧ��
�۸���̼���ơ��������ƺ��Ȼ��ƵĻ�ѧ���ʼ����ӵ�ԭ��ش�
�ܸ���̼���ƵĻ�ѧ���ʺͼ��鷽���ش�
�ݸ��ݵڶ���ʳ����NH4HCO3��Ӧ�Ǹ��ֽⷴӦ���Լ�̼�����Ƶ��ܽ�Ƚ�С����Ϣ��д����ʽ��
��4�����ⷢ���ķ�ӦΪNa2CO3+2HCl�T2NaCl+CO2��+H2O�����������غ㶨�ɼ������Ӧ���ɵĶ�����̼���������ٸ��ݶ�����̼�������ͻ�ѧ����ʽ���㴿����Ʒ��̼���Ƶ������������ô�����Ʒ��̼���Ƶ�����������
����⣺��1��NH3+CO2+H2O=NH4HCO3���ص��ǡ����һ�������ϻ��Ϸ�Ӧ�Ķ�����ص㣬Ϊ���Ϸ�Ӧ��
��2���ٽ���ʹ�����ƴӴ���ˮ��������˵�������Ƶ��ܽ�����¶ȵĽ��Ͷ���С�������¶ȱ仯Ӱ������ԣ�
�ڼ����ɽ������Ӻ����������ӹ��ɵģ�����Ԫ�صļ�Ϊ�������ƣ���ѧʽΪ��Ca��OH��2���������ơ��Ȼ��ơ��Ȼ�þ�������������������У�ֻ���Ȼ�þ�����������ܷ�����Ӧ����������þ�������Ȼ��ƣ�����ʽΪ��Ca��OH��2+MgCl2�TMa��OH��2��+CaCl2��
�ۡ�����II�������У�����B�ε������dz�ȥ�������������ƺ��Ȼ��Ƶģ���ͨ����������ȥ��Ϊ�˱�֤�����������ʣ�Ӧ����̼���ƣ��йط�Ӧ����ʽΪ��CaCl2+Na2CO3�T2NaCl+CaCO3����Ca��OH��2+Na2CO3�T2NaOH+CaCO3����
�ܼ�����Һ��B���Ƿ������ʵ���Ͼ��Ǽ���̼���ƵĴ��ڣ�����Ϊ����һ��ȡ������II�����˺����Һ�������Թ��У������Ȼ�����Һ���۲죬�������ɫ��������̼�����ѹ�������������ȡ������II�����˺����Һ�������Թ��У�����ϡ���ᣬ�۲죬��������ݣ���̼�����ѹ�����
��ʳ����NH4HCO3��Ӧ�Ǹ��ֽⷴӦ�����ݷ�Ӧ�ص㡰���������۲��䡱�жϣ��������Ȼ�狀�̼�����ƣ�̼�����Ƶ��ܽ�Ƚ�С���ᾧ����������Ϊ���������Է���ʽΪ��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
��4���⣺���ɶ�����̼������Ϊ100g+5.6g-103.4g=2.2g
����Ʒ��̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+CO2��+H2O
106 44
x 2.2g
=
x=5.3g
��ô�����Ʒ��̼���Ƶ���������Ϊ
��100%=94.6%
��������Ʒ��̼���Ƶ���������Ϊ94.6%��
�ʴ�Ϊ����1�����ϣ�
��2���ٴ�
��Ca��OH��2��Ca��OH��2+MgCl2�TMa��OH��2��+CaCl2��
��CaCl2+Na2CO3�T2NaCl+CaCO3����Ca��OH��2+Na2CO3�T2NaOH+CaCO3����
�ܷ���һ��ȡ������II�����˺����Һ�������Թ��У������Ȼ�����Һ���۲죬�������ɫ��������̼�����ѹ�����
��������ȡ������II�����˺����Һ�������Թ��У�����ϡ���ᣬ�۲죬��������ݣ���̼�����ѹ�����������������Ҳ�ɣ�
��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
��4���⣺���ɶ�����̼������Ϊ100g+5.6g-103.4g=2.2g
����Ʒ��̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+CO2��+H2O
106 44
x 2.2g
=
x=5.3g
��ô�����Ʒ��̼���Ƶ���������Ϊ
��100%=94.6%
��������Ʒ��̼���Ƶ���������Ϊ94.6%��
��2���ٽ���ʹ�����ƴӴ���ˮ��������˵�������Ƶ��ܽ�����¶ȵĽ��Ͷ���С�������¶ȱ仯Ӱ������ԣ�
�ڼ����ɽ������Ӻ����������ӹ��ɵģ�����Ԫ�صļ�Ϊ�������ƣ���ѧʽΪ��Ca��OH��2���������ơ��Ȼ��ơ��Ȼ�þ�������������������У�ֻ���Ȼ�þ�����������ܷ�����Ӧ����������þ�������Ȼ��ƣ�����ʽΪ��Ca��OH��2+MgCl2�TMa��OH��2��+CaCl2��
�ۡ�����II�������У�����B�ε������dz�ȥ�������������ƺ��Ȼ��Ƶģ���ͨ����������ȥ��Ϊ�˱�֤�����������ʣ�Ӧ����̼���ƣ��йط�Ӧ����ʽΪ��CaCl2+Na2CO3�T2NaCl+CaCO3����Ca��OH��2+Na2CO3�T2NaOH+CaCO3����
�ܼ�����Һ��B���Ƿ������ʵ���Ͼ��Ǽ���̼���ƵĴ��ڣ�����Ϊ����һ��ȡ������II�����˺����Һ�������Թ��У������Ȼ�����Һ���۲죬�������ɫ��������̼�����ѹ�������������ȡ������II�����˺����Һ�������Թ��У�����ϡ���ᣬ�۲죬��������ݣ���̼�����ѹ�����
��ʳ����NH4HCO3��Ӧ�Ǹ��ֽⷴӦ�����ݷ�Ӧ�ص㡰���������۲��䡱�жϣ��������Ȼ�狀�̼�����ƣ�̼�����Ƶ��ܽ�Ƚ�С���ᾧ����������Ϊ���������Է���ʽΪ��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
��4���⣺���ɶ�����̼������Ϊ100g+5.6g-103.4g=2.2g
����Ʒ��̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+CO2��+H2O
106 44
x 2.2g
| 106 |
| 44 |
| x |
| 2.2g |
x=5.3g
��ô�����Ʒ��̼���Ƶ���������Ϊ
| 5.3g |
| 5.6g |
��������Ʒ��̼���Ƶ���������Ϊ94.6%��
�ʴ�Ϊ����1�����ϣ�
��2���ٴ�
��Ca��OH��2��Ca��OH��2+MgCl2�TMa��OH��2��+CaCl2��
��CaCl2+Na2CO3�T2NaCl+CaCO3����Ca��OH��2+Na2CO3�T2NaOH+CaCO3����
�ܷ���һ��ȡ������II�����˺����Һ�������Թ��У������Ȼ�����Һ���۲죬�������ɫ��������̼�����ѹ�����
��������ȡ������II�����˺����Һ�������Թ��У�����ϡ���ᣬ�۲죬��������ݣ���̼�����ѹ�����������������Ҳ�ɣ�
��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
��4���⣺���ɶ�����̼������Ϊ100g+5.6g-103.4g=2.2g
����Ʒ��̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+CO2��+H2O
106 44
x 2.2g
| 106 |
| 44 |
| x |
| 2.2g |
x=5.3g
��ô�����Ʒ��̼���Ƶ���������Ϊ
| 5.3g |
| 5.6g |
��������Ʒ��̼���Ƶ���������Ϊ94.6%��
������ѧ��Դ������������ַ�����������������ҵ�dz��л�ѧ��Ҫ��Ӧ��֮һ���ǿ����ص㣬���漰��ѧ����ʽ����д��������̼�Ͱ���ͨ���˳��ԭ��Ӧʱ����̼�����Ƶ�ԭ���������ܽ�ȵĹ�ϵ���ص����ݣ�

��ϰ��ϵ�д�
�����Ŀ
̼������;�dz��㷺���ǹ�ҵ��������Ҫ�Ļ���ԭ�ϣ���1921���ҹ���ѧ�Һ�°�����һ�������Ĵ�����������--�������Ƽ����
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ���� ��Ӧ������Ӧ���ͣ�
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ������Ҫ��������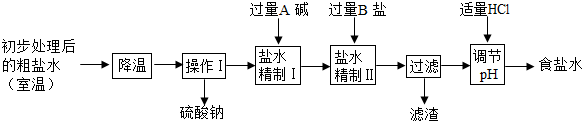
��ͨ������ʹ�����ƴӴ���ˮ����������ԭ�����Ȼ��ƺ������Ƶ��ܽ�����¶ȵı仯����ϴ������ܽ��ͼ����ͼ���м����Ȼ��ƺ������Ƶ��ܽ�����߱仯����ͼ��
�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ�� ���䷴Ӧ��ѧ����ʾΪ ��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ ��
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ�������±���д��������Һ��B���Ƿ������ʵ�鱨�森
�ݲ������ϵ�֪NaCl��NH4HCO3��NaHCO3��NH4Cl��30��ʱ���ܽ�����±���ʾ��
������ܽ�ȱ����ṩ����Ϣ��д���������Ƽ���еĵڶ������ڸ��ֽⷴӦ�Ļ�ѧ����ʽ�� ��
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO3
Na2CO3+H2O+CO2��
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ����
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ������Ҫ��������

��ͨ������ʹ�����ƴӴ���ˮ����������ԭ�����Ȼ��ƺ������Ƶ��ܽ�����¶ȵı仯����ϴ������ܽ��ͼ����ͼ���м����Ȼ��ƺ������Ƶ��ܽ�����߱仯����ͼ��

�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ�������±���д��������Һ��B���Ƿ������ʵ�鱨�森
| ʵ����� | ʵ������ | ʵ����� |
| |
| �¶� | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30�� | 41.1g | 27.0g | 11.1g | 36.3g |
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO3
| ||
̼������;�dz��㷺���ǹ�ҵ��������Ҫ�Ļ���ԭ�ϣ���1921���ҹ���ѧ��
��°�����һ�������Ĵ�����������--�������Ƽ����
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ���ڻ�����Ӧ�����е�______��Ӧ��
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��

����Ҫ�������£�
��ͨ������ʹ�����ƴӴ���ˮ��������˵�������Ƶ��ܽ�����¶ȵı仯��______�����С������
�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ��______���䷴Ӧ��ѧ����ʽΪ______��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ______��______��
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ��д��������Һ��B���Ƿ������ʵ�鷽����______
______��
�ݲ������ϵ�֪NaCl��NH4HCO3��NaHCO3��NH4Cl��30��ʱ���ܽ�����±���ʾ��
| �¶� | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30�� | 41.1g | 27.0g | 11.1g | 36.3g |
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO
 Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2����4���á������Ƽ���ƵõĴ����г������������Ȼ��ƣ�Ϊ�ⶨij������Ʒ��̼���Ƶ�����������С��ͬѧ��ȡ����Ʒ5.6g���뵽ʢ��100g����ϡ������ձ��У���ȫ��Ӧ��Ƶ��ձ��е���Һ����Ϊ103.4g����ô�����Ʒ��̼���Ƶ�����������
̼������;�dz��㷺���ǹ�ҵ��������Ҫ�Ļ���ԭ�ϣ���1921���ҹ���ѧ�Һ�°�����һ�������Ĵ�����������--�������Ƽ����
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ���ڷ�Ӧ������Ӧ���ͣ�
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ������Ҫ��������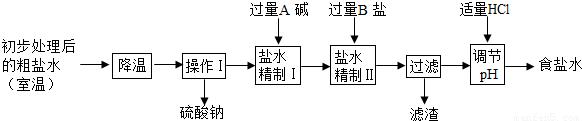
��ͨ������ʹ�����ƴӴ���ˮ����������ԭ�����Ȼ��ƺ������Ƶ��ܽ�����¶ȵı仯����ϴ������ܽ��ͼ����ͼ���м����Ȼ��ƺ������Ƶ��ܽ�����߱仯����ͼ��
�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ�ǣ��䷴Ӧ��ѧ����ʾΪ��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ��
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ�������±���д��������Һ��B���Ƿ������ʵ�鱨�森
�ݲ������ϵ�֪NaCl��NH4HCO3��NaHCO3��NH4Cl��30��ʱ���ܽ�����±���ʾ��
������ܽ�ȱ����ṩ����Ϣ��д���������Ƽ���еĵڶ������ڸ��ֽⷴӦ�Ļ�ѧ����ʽ����
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO3 Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
�������Ƽ���������̣�
��1����һ����Ҫ��ӦΪNH3+CO2+H2O=NH4HCO3�÷�Ӧ���ڷ�Ӧ������Ӧ���ͣ�
��2���ڶ�����ʳ����NH4HCO3��Ӧ��ʳ����Դ��ij����ô�����Ҫ�����Ȼ��ƣ�����������������ƣ��Ȼ��ƺ��Ȼ�þ�������������Ƶõ�����̼��������Ҫ��ʳ��ˮ������Ҫ��������

��ͨ������ʹ�����ƴӴ���ˮ����������ԭ�����Ȼ��ƺ������Ƶ��ܽ�����¶ȵı仯����ϴ������ܽ��ͼ����ͼ���м����Ȼ��ƺ������Ƶ��ܽ�����߱仯����ͼ��

�ڡ�����I�������У������������Ԫ�صļ�Ļ�ѧʽ�ǣ��䷴Ӧ��ѧ����ʾΪ��
�ۡ�����II�������У�����B�ε��йط�Ӧ����ʽΪ��
��Ϊ��֤������II�������й���B�ΰ�����ȫ����ȥ�������±���д��������Һ��B���Ƿ������ʵ�鱨�森
| ʵ����� | ʵ������ | ʵ����� |
| |
| �¶� | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30�� | 41.1g | 27.0g | 11.1g | 36.3g |
��3�������������Ƶ�̼���ƣ���Ӧԭ��Ϊ2NaHCO3
 Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2�� 