题目内容
【题目】某实验小组用下图装置研究CO2的性质。
提示:①忽略块状大理石中杂质对本实验的影响
②碱性碳酸钠溶液与中性氯化钙溶液能发生复分解反应
(1)如下图所示,装入药品,打开K,玻璃管b中反应的化学方程式为__________,导管口处的现象是______________。
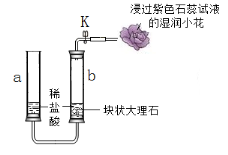
(2)关闭K,一段时间后反应停止。反应能够停止的原因是______________。
(3)反应停止后,向a中滴入酚酞溶液,并加入一定量碳酸钠固体,充分反应后a中溶液呈红色。打开K,待a、b中液面相平后立即关闭K,轻轻振荡b管。一段时间后观察到的现象是____________,最终b中红色褪去,此时b中溶液的溶质可能为__________。
【答案】(1)CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ , 紫色石蕊小花变红;(2)大理石与稀盐酸反应产生CO2,使b管中的气压增大,b中液体被压入a中,大理石与稀盐酸脱离接触,所以反应停止。(3)液面上升,溶液变浑浊。NaCl 或 NaCl、CaCl2 (酚酞)(0或2分)
【解析】
试题分析:(1)打开K,玻璃管b中反应的化学方程式为CaCO3 + 2HCl == CaCl2 +H2O + CO2↑,导管口处的现象是紫色石蕊小花变红;(2)关闭K,一段时间后反应停止。反应能够停止的原因是大理石与稀盐酸反应产生CO2,使b管中的气压增大,b中液体被压入a中,大理石与稀盐酸脱离接触,所以反应停止。(3)反应停止后,向a中滴入酚酞溶液,并加入一定量碳酸钠固体,充分反应后 a中溶液呈红色。打开K,待a、b中液面相平后立即关闭K,轻轻振荡b管。一段时间后观察到的现象是液面上升,溶液变浑浊。,最终b中红色褪去,说明没有碱性物质存在,此时b中溶液的溶质可能为。NaCl 或 NaCl、CaCl2

【题目】小明家有包开启了的小苏打,久置在灶台上方,可能因受热而变质。小明为此开展了探究,请分析其过程完成填空。
【查阅资料】
① 2NaHCO3![]() Na2CO3 + CO2 ↑ + H2O
Na2CO3 + CO2 ↑ + H2O
② NaHCO3 + NaOH = Na2CO3 + H2O
③ 2NaHCO3 + Ca(OH)2 = CaCO3 ↓ + Na2CO3 + 2H2O
④ Ca(HCO3)2 + Na2CO3 = CaCO3 ↓ + 2 NaHCO3
⑤ Na2CO3受热不分解,NaHCO3、Ca(HCO3)2都能溶与水。
【假设猜想】
假设一:小苏打没有变质,化学成分为NaHCO3;
假设二:小苏打完全变质,化学成分为 ;
假设三:小苏打部分变质,化学成分为 。
【实验方案】
可选药品:①Ca(OH)2溶液 ②CaCl2溶液 ③NaOH溶液 ④稀盐酸
实验操作 | 实验现象 | 实验结论 |
操作一:取小苏打样品少量溶于足 量水后,加入过量的 (填药品编 号,下同),观察,如有沉淀,则继续进行下一步操作。 操作二:待操作一中反应充分后过 滤,并在滤液中加入过量的 ,观察。 | 操作一中无沉淀出现 | 假设一成立 |
假设二成立 | ||
假设三成立 |
【问题讨论】
有同学认为,取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断。请评价这种方案是否合理 (填“是”或“否”),理由是 。