��Ŀ����
����Ŀ���ֿ�����һ�����ʵİ�װ��ǩģ�����壬��ͬѧ����������̽����
��1���������ò��������Ŀ���� ��

��2��������±�����֪AgCl��BaSO4��������ˮ����İ�ɫ���壩��
��������� | �жϺͻ�ѧ����ʽ | |
a | ������IΪ�ް�ζ�� | ����Ʒ�в��� �������ƣ��� |
b | �ɲ����������жϣ� | ����Ʒһ������ ���ӣ� |
c | �������Ϊ��ɫ�����������Ϊ������ | ����Ʒ�к��� ��д���ƣ����÷�Ӧ�Ļ�ѧ����ʽΪ �� |
d | �������Ϊ���������������Ϊ��ɫ������ | ����Ʒ�к��� ��д��ѧʽ�����÷�Ӧ�Ļ�ѧ����ʽΪ �� |
��3�������������������õ��ʿ����� ��д��ѧʽ����������������Ϊ����ζ���������������õ��ʿ����� ��ֻдһ�֣���
���𰸡���1��ʹ��Ʒ����ܽ⣻��2��a��̼����泥�b��笠���c������泥���NH4��2SO4+Ba��NO3��2=BaSO4��+2NH4NO3��d��NH4Cl NH4Cl+AgNO3=AgCl��+NH4NO3����3��NH4NO3�����أ�
����������1���������ò��������Ŀ����ʹ��Ʒ����ܽ⣻
��2��a�����ڳ�����̼������ֽ�ų��������д̼�����ζ�����ԣ�������IΪ�ް�ζ������Ʒ�в���̼����泥�
b��������������ܷų����������ԣ�����Ʒ������ʯ�ң��а������ɣ�˵���˸���Ʒһ������笠����ӣ��õ���������Σ�
C��������������ᱵ��Һ��Ӧ���ɲ�����ϡ����İ�ɫ������˵���˸����������泥���Ӧ�ķ���ʽ����NH4��2SO4+Ba��NO3��2=BaSO4��+2NH4NO3��
d�������������������Һ��Ӧ���ɲ�����ϡ����İ�ɫ������˵���˸�������Ȼ�泥���Ӧ�ķ���ʽ��NH4Cl+AgNO3=AgCl��+NH4NO3��
��3�������������������õ��ʿ����� NH4NO3��������������Ϊ����ζ���������������õ��ʲ�����Σ����������أ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ���ÿ�ѧ������ʶ�������ʣ��������̽������գ�
���տ�ѧ��ʶ�Ĺ��̣���ѧ������Ҫ�̺��ڶ����Σ�һ�Ǹ�����ʶ�Σ���Ҫ��Ϊ�˻��֤�ݣ���۲졢Ԥ�⡢ʵ��ȣ�����������ʶ������˼ά���Σ���Ҫ��Ϊ���γɿ�ѧ��ʶ�����ѧ����ѧ��˵����Ƚ���Աȡ�����������ȣ�
��ǰһ�ε�ѧϰ�У�����ͨ��ʵ�顢�۲���ֶ���֤�˺ܶѧ��Ӧ�ķ����������ˡ����ɡ�����Ƚϡ��Աȡ��ȿ�ѧ��һ�㷽����ʶ�˼��ֵ��͵��ᡢ��Σ������������Ϸ�����ʶ�Ȼ�þ��
��1���ù���/����ķ�����ʶ�Ȼ�þ������
��֪���з�Ӧ��
HCl+AgNO3�TAgCl��+HNO3
NaCl2+AgNO3�TAgCl��+NaNO2
BaCl2+2AgNO3�T2AgCl��+Ba��NO3��2��
�����鷴Ӧ�ܹ�������ԭ���� ��
���ɢ��еõ��Ĺ��ɿ������ۡ��Ȼ�þ��ҺҲ�ܸ���������Һ��Ӧ�������õ��� �ķ�����
��2����ʵ��ķ�����ʶ�Ȼ�þ������
��Ҫ��֤��1�����С��Ȼ�þ��ҺҲ�ܸ���������Һ��Ӧ�������ۣ������ʵ�飬ʵ�鷽���ǣ�
ʵ����� | ʵ������ | ���� |
���ۣ��Ȼ�þ��Һ�ܸ���������Һ��Ӧ |
����ʵ��ķ�����ʶ�Ȼ�þ����������
ʵ����� | ʵ������ | ���� |
ȡ�����Ȼ�þ��Һ���Թ��У�Ȼ���ٵμ�2��3����ɫʯ����Һ���� | ʯ����Һ��� | ���ۣ��Ȼ�þ��Һ |
ȡ�����Ȼ�þ��Һ���Թ��У�Ȼ���ٵμ���������Һ | ������ɫ���� | ���ۣ� |
��3������Ҫ��ѧ��ʵ�鷽����������ѧת��������������
�������û�ѧ�仯���������������Ҫ�����ʣ�����شٽ����������ķ�չ����ҵ���Ժ�ˮΪԭ�ϣ�ͨ��һϵ�л�ѧ�仯���Եõ��Ȼ�þ���壻����ˮ�Ȼ�þ��MgCl2��������״̬�£�ͨ�����Եõ�������������þ����Ӧ������ͼ��ʾ����ӻ�ѧ�ӽǻش��������⣺
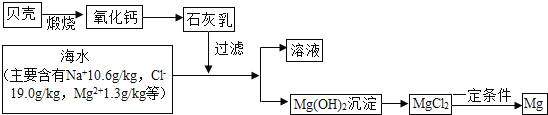
��Ҫʹ��ˮ�е�MgCl2��ȫת��Ϊ����Mg��OH��2������ʯ���飨��Ҫ�ɷ����������ƣ�Ҫ��������ͬѧ���ʵ��ȷ����ˮ�е�MgCl2��ȫ��ת��ΪMg��OH��2��ȡ�ϲ���Һ�������Թ��У������м��� ���۲쵽 ��˵����ˮ��MgCl2��ȫ��ת��ΪMg��OH��2��
��Ҫ����������������þת��Ϊ�Ȼ�þ������ѡ�õ��Լ��� ��
�ۺ�ˮ�б��������Ȼ�þ��������Ӻ�ˮ����ȡMgCl2ʱ��Ҫ������MgCl2��Mg��OH��2��MgCl2����ת�����̵�ԭ�� ��