题目内容
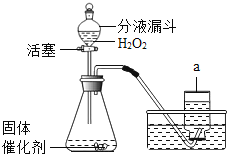
【题目】(6分)在盛有40g溶质质量分数为20%氢氧化钠溶液的烧杯中,用滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中,验证“中和反应会放热”,同时用pH计记录溶液pH的变化,绘制成如图函数图象。
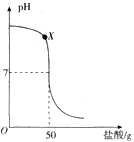
(1)用玻璃棒蘸取X点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有____(填化学式)。
(2)为什么不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”?____。
(3)当pH=7时,求溶液中溶质的质量分数。
【答案】(1)NaCl、NaOH(2分)
(2)氢氧化钠固体溶于水时也会产生热量,这样就无法说明热量来自于中和反应了(1分)
(3)13% (3分,计算出氯化钠质量l分,求出反应后溶液1分,计算出结果1分)
【解析】
试题分析:(1)X点溶液的溶质中,含有氢氧化钠和稀盐酸反应生成的氯化钠及其没有反应的氢氧化钠;用玻璃棒蘸取X点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有氯化钠和氢氧化钠,化学式分别为NaCl、NaOH;
(2)因为氢氧化钠固体溶于水时也会放出热量,这样就无法说明热量来自于中和反应了,所以不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”;
(3)pH=7时,氢氧化钠和稀盐酸恰好完全反应,根据提供的数据可以计算溶液中溶质的质量分数:
设反应生成氯化钠的质量为x,
NaOH+HCl═NaCl+H2O,
40 58.5
40g×20% x
40/58.5=40g×20% /x
x=11.7g,溶液的质量为:40g+50g=90g,
当pH=7时,溶液中溶质的质量分数为11.7g/90g×100%=13%.
答:当pH=7时,溶液中溶质的质量分数为13%.

【题目】某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
实验次数 | 一 | 二 | 三 | 四 |
固体混合物的质量(g) | 20 | 20 | 20 | 20 |
加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
问:
(1)表中m的值为 ;(2分)
(2)原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)