题目内容
 25、如图分别表示A、B、C三种物质的溶解度曲线,试回答:
25、如图分别表示A、B、C三种物质的溶解度曲线,试回答:(1)M 点的含义是
t1℃时A、C的溶解度相等
.(2)温度为t2℃时三种物质的溶解度的大小关系是
A>B>C
.(3)将C物质接近饱和的溶液变为饱和溶液常用的方法是
升高温度
.(4)t2℃的等质量的A、B、C三种物质的饱和溶液分别降温到t1℃析出晶体最多的是
A
物质.(5)在20℃时,向50克的水中加入10克A物质,充分溶解后所得的溶液为
不饱和溶液
(填“饱和溶液”或“不饱和溶液”),若是饱和溶液,以下两空可以不填.若是不饱和溶液,如果要使它成为20℃时的饱和溶液,则可以加入10
克的A物质;或是蒸发25
克的水.(6)若A中混有少量的B物质,分离出A物质常用的方法是
降温结晶
.分析:根据固体物质的溶解度曲线可以:①查出某物质在某温度下的溶解度,从而判断形成的溶液是否饱和,②比较不同物质在同一温度下的溶解度的大小,③判断物质的溶解度随温度变化的变化情况,从而确定饱和溶液和不饱和溶液间的转化方法,确定通过降温还是蒸发溶剂的方法来分离混合物等.
解答:解:(1)M点是A和C的溶解度曲线的交点,即在t1℃时,两者的溶解度相等,故答案为:t1℃时A、C的溶解度相等
(2)根据三种物质的溶解度曲线图不难看出,在t2℃时,三种物质的溶解度大小关系是A>B>C,故答案为:A>B>C
(3)由于C的溶解度随温度的升高而减小,因此若使它的不饱和溶液变为饱和溶液,可采取增加溶质、升高温度或蒸发溶剂的方法,故答案为:升温(合理即可)
(4)由于在这三种物质中,A的溶解度受温度的影响最大且是随温度的降低而减小,因此t2℃的等质量的A、B、C三种物质的饱和溶液分别降温到t1℃析出晶体最多的是A,故答案为:A
(5)由于在20℃时,A的溶解度是40g,即在100g水中最多能够溶解40gA,则在50g水中最多溶解20gA,则10gA溶解在25g水中恰好达到饱和,故答案为:不饱和溶液,10,25
(6)由于A的溶解度随温度的升高而增大,且受温度的影响很大,而B的溶解度受温度的影响很小,因此若提纯混有少量B的A,应采取降温结晶的方法,故答案为:降温结晶
(2)根据三种物质的溶解度曲线图不难看出,在t2℃时,三种物质的溶解度大小关系是A>B>C,故答案为:A>B>C
(3)由于C的溶解度随温度的升高而减小,因此若使它的不饱和溶液变为饱和溶液,可采取增加溶质、升高温度或蒸发溶剂的方法,故答案为:升温(合理即可)
(4)由于在这三种物质中,A的溶解度受温度的影响最大且是随温度的降低而减小,因此t2℃的等质量的A、B、C三种物质的饱和溶液分别降温到t1℃析出晶体最多的是A,故答案为:A
(5)由于在20℃时,A的溶解度是40g,即在100g水中最多能够溶解40gA,则在50g水中最多溶解20gA,则10gA溶解在25g水中恰好达到饱和,故答案为:不饱和溶液,10,25
(6)由于A的溶解度随温度的升高而增大,且受温度的影响很大,而B的溶解度受温度的影响很小,因此若提纯混有少量B的A,应采取降温结晶的方法,故答案为:降温结晶
点评:本题难度不是很大,主要考查了固体溶解度曲线的意义及对固体溶解度概念的理解,以此来解决相关的问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (1)石灰水中的溶质是
(1)石灰水中的溶质是 (2012?闸北区一模)如图分别表示A、B两种物质的溶解度曲线,试回答:
(2012?闸北区一模)如图分别表示A、B两种物质的溶解度曲线,试回答: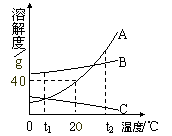
 如图分别表示A、B、C三种物质的溶解度曲线,试回答:
如图分别表示A、B、C三种物质的溶解度曲线,试回答: