题目内容
【题目】(8分)某化学研究性学习小组进行了氨(NH3)的制取和有关性质的探究实验。
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,能使湿润的红色石蕊试纸变蓝色,极易溶于水,浓氨水具有挥发性。加热熟石灰和氯化铵固体混合物可以生成氨气,若要快速产生氨气,可以将浓氨水滴加到生石灰中得到。
请根据有关信息回答下列问题:
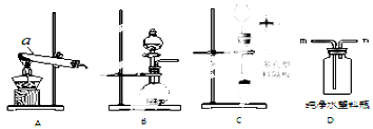
(1)仪器a的名称是 。
(2)氯化铵是化肥中的 ,利用A装置制取氨气的化学方程式是 。
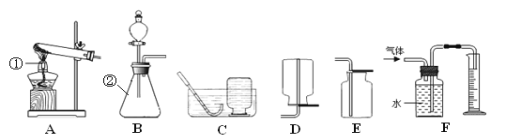
(3)将浓氨水滴加到生石灰中快速产生氨气,发生装置最好是 (选填装置编号)。
(4)研究性学习小组用D装置收集氨气,判断氨气已经收集满的方法是 。
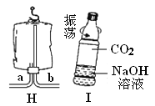
(5)研究性学习小组用下图所示的装置探究氨的性质,观察到脱脂棉团由白色变为红色。该现象涉及到氨气的性质是 (填字母编号)。

A.氨分子是不断运动的 B.浓氨水具有挥发性
C.氨气有刺激性气味 D.氨气的水溶液显碱性
(6)若将制取氨气的熟石灰溶于水形成的饱和溶液置于小烧杯并放入一只大烧杯中(如下图),在大烧杯中加入下列物质,观察到小烧杯中饱和溶液变浑浊,则加入的物质是 (填字母编号)。

A.水和浓硫酸 B.水和氯化钠固体
C.水和硝酸铵固体 D.水和氢氧化钠固体
【答案】(1)试管 (2)氮肥 Ca(OH)2+2NH4Cl△CaCl2+NH3↑+H2O
(3)B (4)将湿润的红色石蕊试纸放在m端,若试纸便蓝色,说明氨气已集满
(5)ABD (6)AD
【解析】
试题分析:(1)常见仪器的识记:试管
(2)氯化铵含营养元素N,属于化肥中的氮肥;利用A装置制取氨气,说明是固体和固体在加热条件下反应,应是加热熟石灰和氯化铵固体混合物,化学方程式是:Ca(OH)2+2NH4Cl△CaCl2+NH3↑+H2O
(3)气体发生装置的选择依据:反应物的状态和反应条件,将浓氨水滴加到生石灰中快速产生氨气,属于固体和液体在常温下反应,故发生装置最好是B
(4)用D装置收集氨气,由于氨气的密度比空气小,故应从短管n端进气,长管m端出气,故判断氨气已经收集满的方法是:将湿润的红色石蕊试纸放在m端,若试纸便蓝色,说明氨气已集满
(5)根据滴有无色酚酞溶液的脱脂棉团变红的现象,可得出的结论有:氨分子是不断运动的,浓氨水具有挥发性,氨气的水溶液显碱性,故选ABD
(6)根据氢氧化钙的溶解度随温度的升高而减低,故要使小烧杯中饱和氢氧化钙溶液析出晶体而变浑浊,就应该升高温度,浓硫酸和氢氧化钠固体溶于水都会放热,使溶液温度升高,故选AD

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】(10分)小明家有包开启了的小苏打,久置在灶台上方,可能因受热而变质。小明为此开展了探究,请分析其过程完成填空。
【查阅资料】①2NaHCO3![]() Na2CO3 + CO2 ↑ + H2O
Na2CO3 + CO2 ↑ + H2O
②2NaHCO3 + Ca(OH)2 = CaCO3 ↓ + Na2CO3 + 2H2O
③Na2CO3受热不分解,NaHCO3能溶与水。
【假设猜想】 假设一:小苏打没有变质,化学成分为 NaHCO3;
假设二:小苏打完全变质,化学成分为 ;
假设三:小苏打部分变质,化学成分为 。
【实验方案】(实验现象2分)
可选药品:①Ca(OH)2溶液 ②CaCl2溶液 ③NaOH溶液 ④稀盐酸
实验操作 | 实验现象 | 实验结论 |
操作一:取小苏打样品少量溶于足量水后,加入过量的 (填药品编号,下同),观察,如有沉淀,则继续进行下一步操作。 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的 ,观察。 | 操作一中无沉淀出现 | 假设一成立 |
假设二成立 | ||
假设三成立 |
【问题讨论】有同学认为,取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断。请评价这种方案是否合理 (填“是”或“否”),理由是 。