题目内容
已知铝能与NaOH溶液反应,化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3X,则X的化学式为 ;NaAlO2中铝元素的化合价为 价.
H2;+3.
解析试题分析:由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X,
反应前 反应后
铝原子 2 2
钠原子 2 2
氧原子 4 4
氢原子 6 0
根据化学变化前后原子的种类、数目不变,可判断物质X的每个分子由2个氢原子构成,则物质X的化学式为H2;设化合物NaAlO2中铝元素的化合价为x,依据化合物中各元素的化合价的代数和为0,则(+1)+x+(﹣2)×2=0,解得x=+3.
考点:质量守恒定律及其应用;有关元素化合价的计算.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
建立宏观、微观和符号之间联系是学习化学的一种方法。
(1)在汞、水、氯化钠三种物质中,由原子直接构成的物质是 。
(2)用化学符号表示:2个水分子 ,3个氮原子 。
(3)乙基雌烯醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O。乙基雌烯醇由 种元素组成,分子中H、O两种元素的质量比为 。
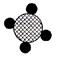
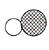
(4)已知:A和B在高温条件下生成C和D,各物质微观示意图如下图所示:
下列说法正确的是 (填数字序号)。
| A.该反应中元素化合价都不变 |
| B.化学变化中分子和原子均可再分 |
| C.4种物质中属于氧化物的是B和C |
| D.若反应后生成1.8gD,则生成C的质量为8.4g |
| A | B | C | D |  |
 |  |  |  |
有限的元素可组成种类繁多的物质.依据表中的元素回答下列问题.
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | C | O | Cl | Mn | Fe |
(1)A溶液在黑色固体B的作用下生成无色气体D,D与生命活动息息相关.A溶液中的溶质用化学式表示为 .
(2)无色气体E与红色固体F在一定条件下反应,得到固体G,反应的化学方程式为 .
(3)将一定量的固体G放入一定量且过量M溶液中,能发生反应,观察到的现象是 .
(4)向(3)所得溶液中加入适量A溶液,溶液变为黄色,且溶质仅有一种,该反应的化学方程式
为 .
 ”表示一个氮分子, 则“
”表示一个氮分子, 则“ ”表示 (填写符号)。
”表示 (填写符号)。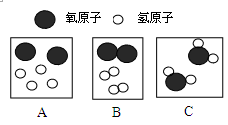
 CO+X,X的化学式是 。
CO+X,X的化学式是 。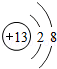 ,用化学符号表示为 .
,用化学符号表示为 .