题目内容
【题目】如图是实验室制取、收集、物质分离的部分装置,请回答下列问题:
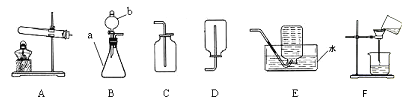
(1)请写出下列仪器的名称a___________;b___________。
(2)实验室中用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式为:___________________,该反应属于_______反应(填化合、分解、氧化之一)。
不能用D装置收集氧气的原因是______________________________。
(3)反应后的混合物中,固体物质的化学式为________ ,可以通过F装置将其分离出来,F装置涉及的操作名称是_________,说出图F中的一条错误_____________________________________
(4)氯酸钾(KClO3)固体在二氧化锰做催化剂并加热的条件下,能较快的分解为氯化钾和氧气,写出该反应的化学方程式_____________________________________________
(5)在加入药品之前,检查B装置气密性的方法是___________________________________
(6)在实验室里常用氯化铵固体与氢氧化钙固体通过加热制取少量氨气,氨气易溶于水,密度小于空气,制取氨气应选用的发生装置为______(填序号,下同),收集氨气应选用的装置为_______ 。
【答案】 锥形瓶 分液漏斗(有错别字不得分) 2H2O2 MnO2 2H2O + O2↑ 分解 氧气的密度大于空气的密度 MnO2 过滤(有错别字不得分) 没有用玻璃棒引流或漏斗下端没有贴近烧杯内壁(说明:填两条的,两条都对得1分,不管填几条,只要有错就不给分) 2KClO3![]() 2KCl+ 3O2↑ 【答题空10】关闭分液漏斗的开关,导气管插入水中,用手握住锥形瓶的外壁,导管口有气泡冒出,证明装置不漏气 A D
2KCl+ 3O2↑ 【答题空10】关闭分液漏斗的开关,导气管插入水中,用手握住锥形瓶的外壁,导管口有气泡冒出,证明装置不漏气 A D
【解析】(1)a仪器为试管;b仪器为集气瓶;
(2)过氧化氢分解生成水和氧气,发生反应的化学方程式为2H2O2![]() 2H2O + O2↑;反应符合“一变多”的特点,属于分解反应;由于氧气的密度大于空气的密度,所以不能用D装置收集氧气;
2H2O + O2↑;反应符合“一变多”的特点,属于分解反应;由于氧气的密度大于空气的密度,所以不能用D装置收集氧气;
(3)二氧化锰作为催化剂反应前后质量和化学性质不变,所以反应后的混合物中,固体物质的化学式为MnO2;F装置涉及的操作为过滤;图中没有用玻璃棒引流或漏斗下端没有贴近烧杯内壁;
(4)氯酸钾(KClO3)固体在二氧化锰做催化剂并加热的条件下,生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl+ 3O2↑;
2KCl+ 3O2↑;
(5)B装置气密性的方法是:关闭分液漏斗的开关,导气管插入水中,用手握住锥形瓶的外壁,导管口有气泡冒出,证明装置不漏气。
(6)实验室里可用氢氧化钙与氯化铵的固体混合物加热制取氨气,是固体加热型反应,则制取氨气所需的气体发生装置为A,氨气极易溶于水,不能用排水法收集,密度小于空气,可以使用向下排空气法收集。