题目内容
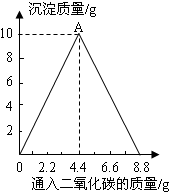
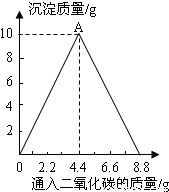
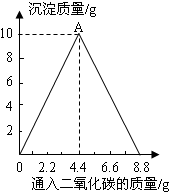 已知反应:CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通人CO2,产生沉淀的质量与通人CO2气体
已知反应:CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通人CO2,产生沉淀的质量与通人CO2气体
的质量的关系如图所示,回答下列问题:
(1)写出OA段反应的化学方程式:______.
(2)至少通入CO2气体质量为______g时,溶液的质量是整个实验过程中溶液质量的最大值(不考虑CO2气体在水中的溶解).
解:由题意,因为“CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水”,故如图所示:溶液先变浑浊后又变澄清.“变浑浊”,是二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀的过程;“后又变澄清”是CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2的过程;
(1)由图可知,OA段的沉淀不断增加,故可写出OA段反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;
(2)溶液质量的增加,是二氧化碳的质量增加;在此过程中,沉淀应全部溶解,溶液的质量达最大值时,即:至少通入CO2气体质量为8.8克时,溶液的质量是整个实验过程中溶液质量的最大值.
故答为:(1)Ca(OH)2+CO2═CaCO3↓+H2O;
(2)8.8克.
分析:由题意,因为“CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水”,故如图所示:开始产生白色沉淀,随着CO2的不断通入沉淀逐渐增多,然后沉淀不断减少,最后完全消失.(或者写溶液先变浑浊后又变澄清)
(1)由图可知,OA段的沉淀不断增加,故可写出OA段反应的化学方程式:为二氧化碳与氢氧化钙溶液的反应;
(2)整个实验过程中溶液质量的增加,是二氧化碳的质量增加,在此过程中,沉淀应全部溶解,质量的增加才会可能达最大值.
点评:掌握化学方程式的书写技巧与方法;了解常见化学反应中的质量关系.
(1)由图可知,OA段的沉淀不断增加,故可写出OA段反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;
(2)溶液质量的增加,是二氧化碳的质量增加;在此过程中,沉淀应全部溶解,溶液的质量达最大值时,即:至少通入CO2气体质量为8.8克时,溶液的质量是整个实验过程中溶液质量的最大值.
故答为:(1)Ca(OH)2+CO2═CaCO3↓+H2O;
(2)8.8克.
分析:由题意,因为“CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水”,故如图所示:开始产生白色沉淀,随着CO2的不断通入沉淀逐渐增多,然后沉淀不断减少,最后完全消失.(或者写溶液先变浑浊后又变澄清)
(1)由图可知,OA段的沉淀不断增加,故可写出OA段反应的化学方程式:为二氧化碳与氢氧化钙溶液的反应;
(2)整个实验过程中溶液质量的增加,是二氧化碳的质量增加,在此过程中,沉淀应全部溶解,质量的增加才会可能达最大值.
点评:掌握化学方程式的书写技巧与方法;了解常见化学反应中的质量关系.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
 25、已知反应:CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通人CO2,产生沉淀的质量与通人CO2气体
25、已知反应:CaCO3+H2O+CO2=Ca(HCO3)2,生成物Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通人CO2,产生沉淀的质量与通人CO2气体