题目内容
【题目】如图是化学实验过程中某些量的变化图像,其中正确的是()
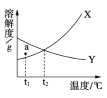
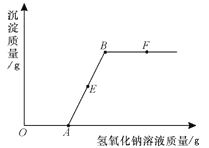
A.向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸 | B.等质量的锌、铁分别和足量的等质量分数的盐酸溶液反应 |
|
|
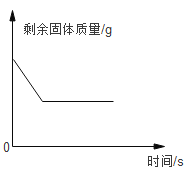
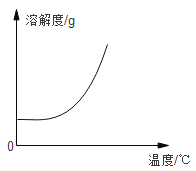
C.在足量的锌粉中加入一定量的CuSO4溶液 | D.一定压强下二氧化碳在水中的溶解度 |
|
|
A.AB.BC.CD.D
【答案】C
【解析】
A、向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸,稀硫酸与氢氧化钠和氢氧化钡都发生反应,氢氧化钠与稀硫酸反应的实质是氢氧根离子与氢离子反应结合生成水,氢氧化钡与稀硫酸反应的实质是氢氧根离子与氢离子反应结合生成水,同时钡离子与硫酸根离子结合生成难溶的硫酸钡,离子之间的结合互相不影响,且硫酸钡不溶于酸和碱,因此两个反应同时发生,反应一开始就有沉淀生成,选项A图不正确;
B、等质量的锌、铁分别和足量的等质量分数的盐酸溶液反应,锌的活动性大于铁,因此反应速率大于铁,且铁产生的氢气大于锌,图中产生的气体质量相等,因此选项B图不正确;
C、在足量的锌粉中加入一定量的CuSO4溶液,锌的活动性大于铜,锌与硫酸铜反应生成铜和硫酸锌,因为锌的相对原子质量大于铜,因此置换出来的固体铜小于参加反应的固体锌,固体质量减小,选项C图正确;
D、气体的溶解度与温度成反比,温度越高,气体在水中的溶解度越小,选项D图不正确。

练习册系列答案
相关题目