题目内容
A~G为实验室中未贴标签的7种溶液.已知7种溶液分别为:澄清的石灰水、氯化钠溶液、硫酸铜溶液、碳酸钠溶液、溶质质量分数为7.3%的盐酸、溶质质量分数均为10%的氢氧化钠溶液和氢氧化钾溶液.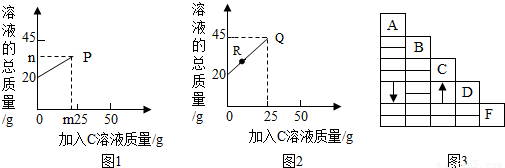
(1)G为蓝色,则G中溶质为(写化学式) .
(2)用pH试纸检测其余溶液的pH,测得E的pH=7,E为 溶液.
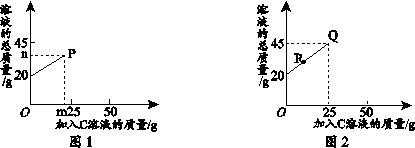
(3)将A、B、C、D、F溶液两两混合,观察到的现象记录如图3所示(图中“-----”代表无明显现象).图中所发生的反应共有 个.写出A与D反应的化学方程式 .
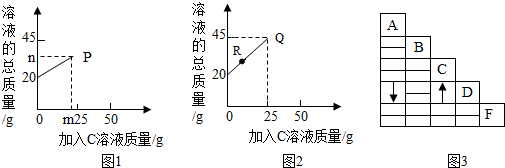
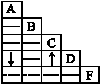
(4)取未鉴别出的两种溶液各20g,分别加入烧杯中,再向烧杯中分别加入C溶液,加入C溶液的质量与烧杯中溶液总质量关系如图所示(已知P、Q两点溶液呈中性).图1中发生反应的化学方程式为 ; 图2中R点所示溶液中溶质为(写化学式) .
【答案】分析:根据题干提供的信息进行分析,(1)G是蓝色溶液,则G是硫酸铜;
(2)E的pH=7,则E是氯化钠溶液;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸;
(4)根据盐酸与氢氧化钠溶液的反应以及盐酸与氢氧化钾溶液反应的质量关系进行分析.
解答:解:(1)G是蓝色溶液,则G是硫酸铜,故填:CuSO4;
(2)E的pH=7,则E是氯化钠溶液,故填:NaCl;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸,B和F是氢氧化钠溶液或氢氧化钾溶液,在图中,A能和C以及D反应,C能和B和F反应,C能和D反应,共发生了5个反应,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故填:5,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)20g10%的氢氧化钠溶液和氢氧化钾溶液中含有溶质的质量为:20g×10%=2g,
HCl+NaOH═NaCl+H2O
36.5 40
HCl+KOH═KCl+H2O
36.5 56
根据反应的化学方程式可以看出,与相同质量的氢氧化钠和氢氧化钾反应,氢氧化钠消耗的盐酸的量多,故图1表示的是氢氧化钾与盐酸的反应,图2表示的是氢氧化钠与盐酸的反应,图2中,R点时氢氧化钠与盐酸未完全反应,还有没参加反应的氢氧化钠,故填:HCl+KOH═KCl+H2O,NaCl、NaOH.
点评:本题为物质推断题,完成此题,关键是根据题干叙述,找准解题突破口,直接得出有关物质的化学式,然后根据题意,结合物质的性质,推断得出其他物质的化学式.
(2)E的pH=7,则E是氯化钠溶液;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸;
(4)根据盐酸与氢氧化钠溶液的反应以及盐酸与氢氧化钾溶液反应的质量关系进行分析.
解答:解:(1)G是蓝色溶液,则G是硫酸铜,故填:CuSO4;
(2)E的pH=7,则E是氯化钠溶液,故填:NaCl;
(3)C和D混合有气体产生,则C和D是盐酸和碳酸钠溶液,D和A混合有沉淀生成,则D是碳酸钠溶液,A是石灰水,C是盐酸,B和F是氢氧化钠溶液或氢氧化钾溶液,在图中,A能和C以及D反应,C能和B和F反应,C能和D反应,共发生了5个反应,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故填:5,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)20g10%的氢氧化钠溶液和氢氧化钾溶液中含有溶质的质量为:20g×10%=2g,
HCl+NaOH═NaCl+H2O
36.5 40
HCl+KOH═KCl+H2O
36.5 56
根据反应的化学方程式可以看出,与相同质量的氢氧化钠和氢氧化钾反应,氢氧化钠消耗的盐酸的量多,故图1表示的是氢氧化钾与盐酸的反应,图2表示的是氢氧化钠与盐酸的反应,图2中,R点时氢氧化钠与盐酸未完全反应,还有没参加反应的氢氧化钠,故填:HCl+KOH═KCl+H2O,NaCl、NaOH.
点评:本题为物质推断题,完成此题,关键是根据题干叙述,找准解题突破口,直接得出有关物质的化学式,然后根据题意,结合物质的性质,推断得出其他物质的化学式.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目