题目内容
下列有关分子、原子和离子的说法正确的是( )
| A、保持氮气化学性质的粒子是氮分子 |
| B、原子的质子数决定元素的化学性质 |
| C、氯化钠是由原子构成的化合物 |
| D、原子可以构成分子,但不可形成离子 |
考点:分子的定义与分子的特性,分子、原子、离子、元素与物质之间的关系,原子的定义与构成,分子和原子的区别和联系
专题:物质的微观构成与物质的宏观组成
分析:A、根据分子是保持物质化学性质的一种粒子分析;
B、根据决定元素的化学性质的微粒考虑;
C、根据氯化钠是由离子构成的离子化合物分析;
D、根据原子的性质特点分析
B、根据决定元素的化学性质的微粒考虑;
C、根据氯化钠是由离子构成的离子化合物分析;
D、根据原子的性质特点分析
解答:解:A、分子是保持物质化学性质的一种粒子,因此,保持氮气化学性质的粒子氮分子,故A正确;
B、原子的核内质子数决定元素的种类,而不是决定元素的化学性质,元素的化学性质由原子的最外层电子数决定,故B错;
C、氯化钠是由钠离子和氯离子构成的离子化合物,故C错;
D、原子通过得失电子可以形成离子,故D错.
故答案为:A
B、原子的核内质子数决定元素的种类,而不是决定元素的化学性质,元素的化学性质由原子的最外层电子数决定,故B错;
C、氯化钠是由钠离子和氯离子构成的离子化合物,故C错;
D、原子通过得失电子可以形成离子,故D错.
故答案为:A
点评:通过回答本题知道了分子的特点,决定元素种类的微粒,构成物质的基本微粒等内容.

练习册系列答案
相关题目
有一种含CaCO3与CaO的混合物,取该混合物16g,经高温煅烧后,将剩余固体投入足量水中,固体全部溶解生成Ca(OH)2,生成的Ca(OH)2质量为22.2g,则原混合物中钙元素质量分数为( )
| A、40% | B、50% |
| C、75% | D、45% |
小明为探究金属与盐的反应,将一定质量的金属粉末M放入AgNO3与Cu(NO3)2的混合溶液中,充分反应后发现,溶液呈现无色,溶液底部有少量固体粉末;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中无沉淀产生.结合实际现象判断,小明得出的以下结论错误的是( )
| A、滤液中一定没有银离子 |
| B、滤渣中一定含有金属Ag |
| C、滤渣中一定含有单质铜 |
| D、加入的金属M可能是单质铁 |
下列物质的用途不正确的是( )
A、 压缩天然气做燃料 |
B、 用金刚石切割玻璃 |
C、 氮气用于食品防腐 |
D、 二氧化碳气体人工降雨 |
与其他三种有本质区别的一种性质是( )
| A、颜色 | B、状态 | C、硬度 | D、可燃性 |
下列实验操作,错误的是( )
A、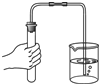 |
B、 |
C、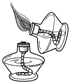 |
D、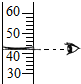 |
