题目内容
【题目】根据如图所示装置回答有关问题:
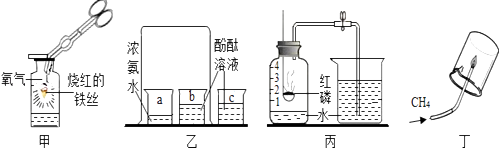
(1)Ⅰ.如图1所示装置 
若用装置B排水收集氧气,气体从(填“a”或“b”)导管通入瓶内;瓶底留少量水进行装置C中的实验,水的作用是 .
(2)对比装置D和C,可以得出的结论是 .
(3)某同学连接A,E,F进行实验,A中所加药品不同,F中所加药品相同.
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则A中反应的化学方程式为;E中蜡烛熄灭,说明A中产生的气体所具有的性质为 .
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为 .
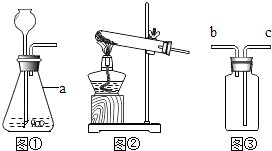
(4)Ⅱ.二氧化碳是一种与人类生产、生活有密切关系的气体. 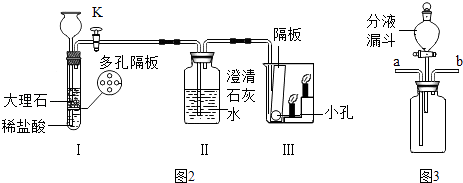
甲同学利用如图2装置对二氧化碳的性质进行验证.
关闭K,装置Ⅰ中能观察到的现象是;
作为制取二氧化碳的发生装置,装置Ⅰ的优点是 .
(5)乙同学利用如图3装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是(填序号,可重复选用).
①从b端通氮气 ②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳 ④从分液漏斗中滴加适量水.
【答案】
(1)b;防止铁的熔化物温度过高而炸裂集气瓶
(2)可燃物达到着火点才能燃烧
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳既不能燃烧,也不能支持燃烧;2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(4)稀盐酸被压入长颈漏斗中,固液分离;可以控制反应的发生和停止
(5)②①④③
【解析】解:(1)Ⅰ若用装置B排水收集氧气,气体从短管进入,因为氧气的密度比水小;瓶底留少量水进行装置C中的实验,水的作用是:防止铁的熔化物温度过高而炸裂集气瓶;所以答案是:b;防止铁的熔化物温度过高而炸裂集气瓶;(2)对比装置D和C,可以得出的结论是:可燃物达到着火点才能燃烧;所以答案是:可燃物达到着火点才能燃烧;(3)若实验时E中蜡烛熄灭,F中溶液变浑浊,说明制取的气体是二氧化碳,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;E中蜡烛熄灭,说明A中产生的气体所具有的性质为:二氧化碳既不能燃烧,也不能支持燃烧;若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则制取的气体是氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;所以答案是:①CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳既不能燃烧,也不能支持燃烧;②2H2O2 ![]() 2H2O+O2↑;(4)Ⅱ甲同学利用如图2装置对二氧化碳的性质进行验证,关闭K,装置Ⅰ中能观察到的现象是:稀盐酸被压入长颈漏斗中,固液分离;作为制取二氧化碳的发生装置,装置Ⅰ的优点是:可以控制反应的发生和停止;所以答案是:稀盐酸被压入长颈漏斗中,固液分离;可以控制反应的发生和停止;(5)乙同学利用如图3装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是:②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中,①从b端通氮气,④从分液漏斗中滴加适量水,③从a端通二氧化碳,所以答案是:②①④③;
2H2O+O2↑;(4)Ⅱ甲同学利用如图2装置对二氧化碳的性质进行验证,关闭K,装置Ⅰ中能观察到的现象是:稀盐酸被压入长颈漏斗中,固液分离;作为制取二氧化碳的发生装置,装置Ⅰ的优点是:可以控制反应的发生和停止;所以答案是:稀盐酸被压入长颈漏斗中,固液分离;可以控制反应的发生和停止;(5)乙同学利用如图3装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是:②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中,①从b端通氮气,④从分液漏斗中滴加适量水,③从a端通二氧化碳,所以答案是:②①④③;
【考点精析】根据题目的已知条件,利用二氧化碳的化学性质和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;注意:a、配平 b、条件 c、箭号.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】如图的实验可用于研究燃烧的条件(夹持固定装置略去). 
已知:白磷的着火点为40℃,红磷的着火点为240℃.
(1)图1的实验中,分别用玻璃棒蘸取酒精和水,在酒精灯火焰上加热,片刻后移开,实验现象如下:
实验用品 | 实验现象 |
蘸有酒精的玻璃棒 | 产生火焰 |
蘸有水的玻璃棒 | 无明显变化 |
此现象能够说明燃烧应具备的条件是 , 实验中发生反应的化学方程式为 .
(2)图2的实验中,a、b处放有少量白磷,c处放有少量红磷.观察到a处白磷燃烧、c处红磷不燃烧,此现象能够说明燃烧应具备的条件是;观察到a处白磷燃烧、b处白磷不燃烧,此现象能够说明燃烧应具备的条件是 .
(3)相比于教材中的实验装置(图3),图2实验装置的优点是 .