题目内容
据报道,广东省某市一化工厂一个容量为2吨的浓硫酸储罐底部突然裂开,造成质量分数为98%的浓硫酸全部泄露,严重威胁附近居民的安全,火速赶到现场的防化人员挖坑导酸,并紧急调来10吨碱溶液中和硫酸,排除险情,请计算,这次抢险至少要消耗多少吨固体烧碱?
【答案】分析:先算出纯硫酸的质量,然后写出化学方程式并代入计算即可.
解答:解:纯硫酸的质量=2×98%=1.96吨,设需要烧碱的质量是X吨.
2NaOH+H2SO4═Na2SO4+2H2O
80 98
X 1.96t
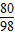 =
=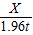
得X=1.6t
答:这次抢险至少要消耗1.6吨烧碱.
点评:掌握化学方程式计算的格式和规范,看清题目,要的是固体烧碱的质量,不是溶液.
解答:解:纯硫酸的质量=2×98%=1.96吨,设需要烧碱的质量是X吨.
2NaOH+H2SO4═Na2SO4+2H2O
80 98
X 1.96t
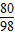 =
=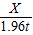
得X=1.6t
答:这次抢险至少要消耗1.6吨烧碱.
点评:掌握化学方程式计算的格式和规范,看清题目,要的是固体烧碱的质量,不是溶液.

练习册系列答案
相关题目