题目内容
下列实验的操作正确的是
A.给试管里的液体加热之初,要不时地移动试管
B.证明二氧化碳能溶解于水时,先在软质塑料瓶内加水,后通入二氧化碳
C.测定溶液的酸碱度时,先将pH试纸润湿,然后用玻璃棒将待测液滴到试纸上
D.检验混合气体中含有CO和CO2:先通过灼热氧化铜,再通过澄清石灰水
 阅读快车系列答案
阅读快车系列答案实验课上李老师指出,在金属活动性顺序里,位于前面的金属能把位于后面的金属从它的盐溶液中置换出来,但钾、钙、钠等除外。全班学生很好奇,于是李老师补做了金属钠与硫酸铜溶液反应的实验。
[进行实验]取一块绿豆大小的金属钠,放入盛有20mL硫酸铜溶液的烧杯中,发现金属钠浮在液面上,熔成闪亮小球,四处游动,产生大量气体,溶液中出现了蓝色絮状沉淀,并没有出现紫红色的铜,一会儿,部分沉淀渐渐变黑。
[提出问题]金属钠与硫酸铜溶液反应后的产物是什么?
[查阅资料]①钠能与水反应生成种能使无色酚酞变红的溶液, 同时放出气体。
②氢氧化铜受热至60-80°C变暗,温度再高分解为相应的金属氧化物和水。氢氧化物和金属氧化物均能与稀酸反应。
[探究一]生成的气体是什么?
(1)小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,将导管另一端通入肥皂水中,将燃着的木条靠近飘起的肥皂泡。有爆鸣声,说明生成的气体是_______。
[探究二]生成的沉淀是什么?
(2)[猜想假设]最后的沉淀中含Cu(OH)2和______,一定不含有Cu。
(3)[实验验证]填写相应实验药品的实验现象:
实验步骤 | 实验现象 | 结论 |
将锥形瓶内反应后的物质过滤,向滤出的固体中加入足量的_______,并加热 | ________。 | 沉淀中不含有Cu |
(4)[实验結论]通过实验,小明同学得出结论:钠加入到硫酸铜溶液中会先与水反应,生成物再与硫酸铜反应生成氢氧化铜。试写出金属钠与水反应的化学方程式:________。
(5)[思考交流]后来部分沉淀渐渐变黑的原因可能是_______。


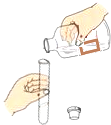 取用液体 B.
取用液体 B. 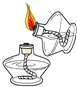 点燃酒精灯
点燃酒精灯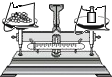 称量氯化钠固体 D.
称量氯化钠固体 D.  加热固体
加热固体 连接仪器
连接仪器 滴加液体
滴加液体 取用石灰石
取用石灰石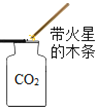 CO2验满
CO2验满