题目内容
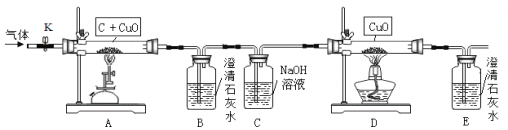
【题目】某化学小组的同学在老师的指导下,设计如下装置验证碳酸钙的性质的同时,探究氧化钙与二氧化碳在加热的条件下是否也能发生反应生成碳酸钙。
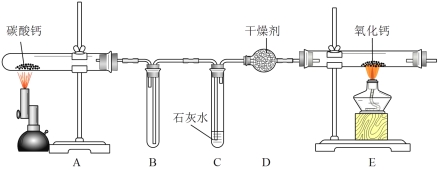
①C中的现象是(15)。装置 B的作用是(16)。
②实验后小组同学对E中固体的成分进行探究。
【猜想与假设】
E中的固体可能为①氧化钙;②氧化钙与碳酸钙; ③碳酸钙
【进行实验】
甲同学取一定量的E中固体于试管中,并加入一定量的水,振荡,有白色不溶物,甲同学认为试管中的固体为碳酸钙,即猜想③成立。乙同学认为上述实验不足以证明猜想③成立,其理由是(17)。他又重新进行实验,证明了猜想②成立,他的实验操作及现象为(18)。
③如果A中碳酸钙的质量为200克,则完全分解产生二氧化碳的物质的量是多少?(写出计算过程)
【答案】①(15)石灰水变浑浊(16)防止石灰水倒流,使试管炸裂
②(17)氧化钙和水反应生成的氢氧化钙是微溶物质,加入一定的水后,有白色不溶物也可能是氢氧化钙。(18)分别取样品2份,1份加入水中,再滴加酚酞,如果变红,表示有氧化钙
③2mol
【解析】
试题分析:碳酸钙受热分解生成二氧化碳,所以C中的现象是石灰水变浑浊,装置B的作用是起到了缓冲的作用,防止石灰水倒流,使试管炸裂,氧化钙和水反应生成的氢氧化钙是微溶物质,加入一定的水后,有白色不溶物也可能是氢氧化钙。分别取样品2份,1份加入水中,再滴加酚酞,如果变红,表示有氧化钙,另一份中滴加稀盐酸如果有气泡产生,说明有碳酸钙。设:产生Xmol的二氧化碳,
CaCO3高温CaO+CO2↑
1001
200克X列比例式得:100:1=200克:Xmol解得:X=2mol

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目