题目内容
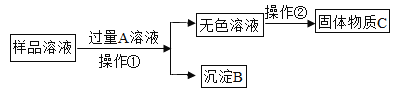
【题目】下图为某些物质间的转化关系。甲、乙、丙均为气体,乙有毒,F是常见金属。A是大理石的主要成分,反应①是自然界中普遍存在的反应,I是黑色固体。部分反应物和生成物已略去。

(1)化学式:D______,H______。
(2)反应③、⑤的化学方程式:③___________, ⑤______。
(3)反应②在医学上可用于_____病的检查。
(4)生活中防止反应④发生,可采取的措施是_________。
【答案】C Cu(OH)2 ![]()
 糖尿病 保持表面洁净干燥
糖尿病 保持表面洁净干燥
【解析】
甲、乙、丙均为气体,A是大理石的主要成分,A是碳酸钙,碳酸钙高温生成氧化铜和二氧化碳,甲是二氧化碳,B是氧化钙,I是黑色固体,乙有毒,乙是一氧化碳,F是常见金属,二氧化碳和D会生成一氧化碳,D是碳,F和过氧化氢溶液、稀硫酸反应生成蓝色溶液,蓝色溶液是硫酸铜,硫酸铜和氢氧化钙(氧化钙与溶液中的水反应生成)反应生成氢氧化铜沉淀,H是氢氧化铜沉淀,氢氧化铜加热会生成氧化铜和水,I是氧化铜,一氧化碳和氧化铜高温生成红色沉淀,红色沉淀是氧化亚铜,铜、水、二氧化碳和氧气反应生成碱式碳酸铜,C是碱式碳酸铜,丙是氧气,甲是二氧化碳,E是水,二氧化碳和水反应生成葡萄糖和氧气,G是葡萄糖。
(1)二氧化碳和D会生成一氧化碳,D是碳,硫酸铜和氢氧化钙反应生成氢氧化铜沉淀,H是氢氧化铜沉淀,故化学式D是C,H是Cu(OH)2。
(2)反应③铜、过氧化氢和硫酸反应生成硫酸铜和水,反应的化学方程式为![]() ,反应⑤是一氧化碳和氧化铜在高温的条件下生成氧化亚铜和二氧化碳,反应的化学方程式为
,反应⑤是一氧化碳和氧化铜在高温的条件下生成氧化亚铜和二氧化碳,反应的化学方程式为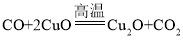 。
。
(3)G是葡萄糖和H是氢氧化铜沉淀加热生成氧化亚铜,反应②在医学上可用于糖尿病的检查。
(4)反应④是铜、水、二氧化碳和氧气反应生成碱式碳酸铜,生活中防止反应④发生,可采取的措施是保持表面洁净干燥。

【题目】以石灰浆为原料制备KClO3的流程如下:
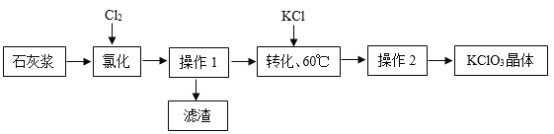
(1)过程中用石灰浆而不用石灰水的原因是_____。
(2)“氯化”反应为6Ca(OH)2+6Cl2=Ca(ClO3)2+5X+6H2O。则X的化学式为____;为提高Cl2转化率,可行措施有____(填序号)。
A 适当减缓通入Cl2速率
B 充分搅拌浆料
C 加水使Ca(OH)2完全溶解
(3)下表是60℃时相关物质的溶解度。转化时加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,原因是_____。
物质 | KCl | KClO3 | Ca(ClO3)2 | CaCl2 |
溶解度 | 43 | 24 | 62 | 70 |
【题目】将一定量的丙醇(C3H8O)和氧气置于一个密封的容器中引燃,测得反应前后各物质的质量如表。下列说法错误的是( )
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 14.8 | 0 | 0.4 | 0 |
反应后质量/g | 0 | 2 | 7.2 | 9.2 | a |
A. 表中a的值为2.8
B. 参加反应的氧气和生成二氧化碳的质量比为16:11
C. X中一定含碳元素、氧元素
D. 该反应属于分解反应