题目内容
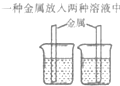
 (2011?本溪)一种“环保石头纸”开始被人们使用,其主要成分是碳酸钙.某班同学对它产生了浓厚的兴趣,把“环保石头纸”带到实验室,完成了如右图所示的两个实验.请回答问题:
(2011?本溪)一种“环保石头纸”开始被人们使用,其主要成分是碳酸钙.某班同学对它产生了浓厚的兴趣,把“环保石头纸”带到实验室,完成了如右图所示的两个实验.请回答问题:(1)实验一:试管中产生大量的气泡,烧杯中澄清的石灰水变浑浊,请写出“环保石头纸”与稀盐酸发生反应的化学方程式
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
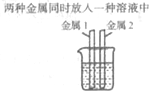
(假设“环保石头纸”中的其他成分既不溶于水,又不与盐酸发生反应);(2)实验二:试管中有白色沉淀产生.小刚同学想探究该实验反应后溶液中溶质的成分.
提出猜想:猜想①:NaCl、CaCl2和HCl;猜想②:NaCl;猜想③:NaCl和CaCl2.
同学们经过讨论排除了猜想
①
①
,理由是稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存)
稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存)
.有同学认为小刚的猜想不全面,又提出猜想④:NaCl和Na2CO3,并通过实验验证了该猜想成立.请你将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| 取实验二反应后的上层清液少量于试管中,滴加少量 稀盐酸 (或Ca(OH)2溶液, 或CaC2l溶液, 或酚酞溶液,合理即可) 稀盐酸 .(或Ca(OH)2溶液, 或CaC2l溶液, 或酚酞溶液,合理即可) |
有气泡产生; (或产生白色沉淀; 或产生白色沉淀; 或溶液变红色合理即可) 有气泡产生; (或产生白色沉淀; 或产生白色沉淀; 或溶液变红色合理即可) |
猜想④成立 |
不能
不能
(填“能”或“不能”)直接倒入下水道.分析:(1)根据石头纸的主要成分是CaCO3,杂质不溶于水,不与盐酸反应,依据书写化学方程式的步骤:写配注等,写出反应方程式;
(2)根据实验一反应后溶液中溶质一定有CaCl2,可能含HCl,实验二中有白色沉淀产生,说明实验二溶液中不可能含HCl;进行分析解答;
碳酸盐与稀盐酸反应生成相应的氯化物、水和二氧化碳气体(即碳酸根离子的检验方法),(或碳酸钙沉淀或碳酸钠显碱性),进行解答;
(3)根据不能倒未经处理的化学废液,主要是为了防止对人造成损害,其次是防止对自然环境造成损害,像强酸、强碱都要中和后倒掉,进行分析解答.
(2)根据实验一反应后溶液中溶质一定有CaCl2,可能含HCl,实验二中有白色沉淀产生,说明实验二溶液中不可能含HCl;进行分析解答;
碳酸盐与稀盐酸反应生成相应的氯化物、水和二氧化碳气体(即碳酸根离子的检验方法),(或碳酸钙沉淀或碳酸钠显碱性),进行解答;
(3)根据不能倒未经处理的化学废液,主要是为了防止对人造成损害,其次是防止对自然环境造成损害,像强酸、强碱都要中和后倒掉,进行分析解答.
解答:解:(1)根据石头纸的主要成分是CaCO3,杂质不溶于水,不与盐酸反应,依据书写化学方程式的步骤:写配注等,因此环保石头纸”与稀盐酸发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)根据实验一反应后溶液中溶质一定有CaCl2,可能含HCl,实验二中有白色沉淀产生,说明实验二溶液中不可能含
HCl;因此排除了猜想①;原因:稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存);
碳酸盐与稀盐酸反应生成相应的氯化物、水和二氧化碳气体(即碳酸根离子的检验方法),(或碳酸钙沉淀或碳酸钠显碱性),
(3)根据不能倒未经处理的化学废液,主要是为了防止对人造成损害,其次是防止对自然环境造成损害,
所以实验结束后,未经处理的废液 不能 直接倒入下水道.
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)①; 稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存等,合理即可);
(3)不能.
(2)根据实验一反应后溶液中溶质一定有CaCl2,可能含HCl,实验二中有白色沉淀产生,说明实验二溶液中不可能含
HCl;因此排除了猜想①;原因:稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存);
碳酸盐与稀盐酸反应生成相应的氯化物、水和二氧化碳气体(即碳酸根离子的检验方法),(或碳酸钙沉淀或碳酸钠显碱性),
| 实验操作 | 实验现象 |
| 稀盐酸; (或Ca(OH)2溶液 或CaC2l溶液 或酚酞溶液,合理即可) |
有气泡产生; (或产生白色沉淀, 或产生白色沉淀 或溶液变红色,合理即可) |
所以实验结束后,未经处理的废液 不能 直接倒入下水道.
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)①; 稀盐酸能与碳酸钙发生反应(或碳酸钙与稀盐酸不能共存等,合理即可);
| 实验操作 | 实验现象 |
| 稀盐酸; (或Ca(OH)2溶液 或CaC2l溶液 或酚酞溶液,合理即可) |
有气泡产生; (或产生白色沉淀, 或产生白色沉淀 或溶液变红色,合理即可) |
点评:本题考查学生书写化学方程式,及碳酸根的鉴别方法,以及试验室废液的处理方法,不但使学生掌握了知识还培养了学生的环保意识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2011?本溪)A、B、C是初中化学常见的物质,它们之间的转化关系如下图所示(所需反应条件已略去).据图回答问题:
(2011?本溪)A、B、C是初中化学常见的物质,它们之间的转化关系如下图所示(所需反应条件已略去).据图回答问题: