题目内容
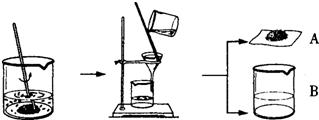
 据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:【提出问题1】固体A中的成分是什么?
【查阅资料】
①CaCO3
| ||
②碳酸钾与碳酸钠性质相似,在溶液中都能与氢氧化钙发生复分解反应.
【猜想与假设】甲同学:只有CaCO3;乙同学:CaCO3、Ca(OH)2;丙同学:CaCO3、CaO
甲、乙两位同学认为丙同学的猜想不合理,理由是
【实验与探究】
甲、乙同学为了验证各自的猜想,分别进行了下述实验:
| 实验操作 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸 | 有气泡产生 | 自己的猜想正确 |
| 乙同学: |
自己的猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】猜想1:KOH、K2CO3;猜想2:KOH、Ca(OH)2;猜想3:KOH
【表达与交流】结合上述实验,同学们讨论确定了猜想
分析:由题目的信息可知:甲、乙两位同学认为丙同学的猜想不合理,理由是生石灰和水反应生成熟石灰,因此氧化钙不存在;甲同学:取少量固体于试管中,向其中加入稀盐酸,有气泡产生,他的猜想不一定正确,因为CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3.乙同学:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液,滤液变为红色,说明是碳酸钙和氢氧化钙的混合物,因此乙同学的猜想正确;结合上述实验,同学们讨论确定了猜想2是正确的,因为反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2;为了得到纯净的氢氧化钾,只要把过量的氢氧化钙除去即可,氢氧化钙可以用适量的碳酸钾除去,氢氧化钙与碳酸钾反应生成碳酸钙白色沉淀和氢氧化钾,配平即可.
解答:解:【猜想与假设】甲、乙两位同学认为丙同学的猜想不合理,理由是生石灰和水反应生成熟石灰,因此氧化钙不存在,故答案为:CaO+H2O=Ca(OH)2
【实验与探究】甲同学:取少量固体于试管中,向其中加入稀盐酸,有气泡产生,他的猜想不一定正确,因为CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3.乙同学:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液,滤液变为红色,说明是碳酸钙和氢氧化钙的混合物,因此乙同学的猜想正确;故答案为:实验操作:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液.实验现象:滤液变为红色
【反思与评价】甲同学的实验不能证明他的猜想,他的理由是:CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3,故答案为:CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3
【表达与交流】结合上述实验,同学们讨论确定了猜想2是正确的,因为反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2;为了得到纯净的氢氧化钾,只要把过量的氢氧化钙除去即可,氢氧化钙可以用适量的碳酸钾除去,氢氧化钙与碳酸钾反应生成碳酸钙白色沉淀和氢氧化钾,配平即可;故答案为:2;反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2.
Ca(OH)2+K2CO3═CaCO3↓+2KOH
【实验与探究】甲同学:取少量固体于试管中,向其中加入稀盐酸,有气泡产生,他的猜想不一定正确,因为CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3.乙同学:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液,滤液变为红色,说明是碳酸钙和氢氧化钙的混合物,因此乙同学的猜想正确;故答案为:实验操作:取少量固体于试管中,加水溶解后过滤,向滤液中加入酚酞溶液.实验现象:滤液变为红色
【反思与评价】甲同学的实验不能证明他的猜想,他的理由是:CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3,故答案为:CaCO3和Ca(OH)2混合物加入盐酸也会有气体产生,所以不能证明固体中只有CaCO3
【表达与交流】结合上述实验,同学们讨论确定了猜想2是正确的,因为反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2;为了得到纯净的氢氧化钾,只要把过量的氢氧化钙除去即可,氢氧化钙可以用适量的碳酸钾除去,氢氧化钙与碳酸钾反应生成碳酸钙白色沉淀和氢氧化钾,配平即可;故答案为:2;反应后一定有KOH生成,上述实验中乙同学证明了固体含有Ca(OH)2,则溶液中一定存在溶解的Ca(OH)2.
Ca(OH)2+K2CO3═CaCO3↓+2KOH
点评:本题属于实验探究题,要注意由实验现象得出正确的结论,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.本考点主要出现在实验题中.

练习册系列答案
相关题目
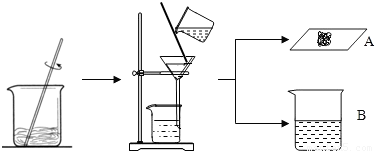
据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
【提出问题1】固体A中的成分是什么?
【猜想与假设】甲同学:只有CaCO3 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
【反思与评价】小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是(2)______;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3 丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了(3)______同学猜想正确,理由是(4)______.
为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为(5)______,小组同学通过相应的实验操作最终制得了氢氧化钾.
【提出问题1】固体A中的成分是什么?

【猜想与假设】甲同学:只有CaCO3 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 自己的猜想正确 |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加(1)______ | 溶液由无色变为红色 | 自己的猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3 丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了(3)______同学猜想正确,理由是(4)______.
为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为(5)______,小组同学通过相应的实验操作最终制得了氢氧化钾.