题目内容
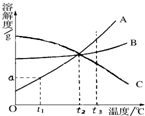 如图是 A、B、C三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法不正确的是( )
如图是 A、B、C三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法不正确的是( )分析:A、根据在t1℃时,A、B、C三种固体物质的溶解度分析;
B、根据A的溶解度随温度的变化分析;
C、根据A、B、C三种固体物质的溶解度随温度的变化分析;
D、根据A、C两种固体物质的溶解度随温度的变化分析.
B、根据A的溶解度随温度的变化分析;
C、根据A、B、C三种固体物质的溶解度随温度的变化分析;
D、根据A、C两种固体物质的溶解度随温度的变化分析.
解答:解:A、由A、B、C三种固体物质的溶解度曲线可知,在t1℃时,A的溶解度是ag,B、C的溶解度大于ag,所以,将A、B、C各a g放入100g水中,充分搅拌所得溶液溶质质量分数均相等.故A正确;
B、由于A的溶解度随温度的升高而增大.所以,t1℃时,取50gA的饱和溶液,将温度升高到t2℃,此时溶液中A的质量分数不变.故B不正确;
C、由于A的溶解度随温度的升高而明显增大,B的溶解度随温度的升高而增大幅度不大,C的溶解度随温度的升高而减小.所以,t3℃时,取相同质量的A、B、C三种饱和溶液降温到t1℃,析出晶体最多的是A,没有晶体析出并变成不饱和溶液的是C.故C正确;
D、由于由于A的溶解度随温度的升高而明显增大,C的溶解度随温度的升高而减小.所以,从A与少量C的混合物中提纯A,可用降温结晶的方法.故D正确.
故选B.
B、由于A的溶解度随温度的升高而增大.所以,t1℃时,取50gA的饱和溶液,将温度升高到t2℃,此时溶液中A的质量分数不变.故B不正确;
C、由于A的溶解度随温度的升高而明显增大,B的溶解度随温度的升高而增大幅度不大,C的溶解度随温度的升高而减小.所以,t3℃时,取相同质量的A、B、C三种饱和溶液降温到t1℃,析出晶体最多的是A,没有晶体析出并变成不饱和溶液的是C.故C正确;
D、由于由于A的溶解度随温度的升高而明显增大,C的溶解度随温度的升高而减小.所以,从A与少量C的混合物中提纯A,可用降温结晶的方法.故D正确.
故选B.
点评:本题难度不是很大,会根据固体溶解度曲线所表示的意义及溶解度随温度变化的情况解决相关的问题,培养学生解决问题的能力.

练习册系列答案
相关题目
 33、如图是a、b、c三种固体物质的溶解度曲线.
33、如图是a、b、c三种固体物质的溶解度曲线.
 (2007?怀柔区一模)如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( )
(2007?怀柔区一模)如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( ) (2012?大田县质检)如图是A、B、C三种固体物质的溶解度曲线图,请回答:
(2012?大田县质检)如图是A、B、C三种固体物质的溶解度曲线图,请回答: 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: