题目内容
【题目】同学们通过化学学习,了解了很多有关金属材料的知识,请你运用所学解决(或解释)以下问题。
(1)“沙里淘金”说明黄金在自然界中能够以________(填“单质”或“化合物”)形式存在。
(2)铁比金活泼,因此钢铁易腐蚀.工业生产中常对钢铁零件“发蓝”处理,以减缓其腐蚀。所谓“发蓝”,就是将钢铁零件等进行氧化处理,使其表面形成一层致密的蓝黑色氧化膜,其处理过程可表示如下:
![]()
经“发蓝”处理后的钢铁零件表面上的蓝黑色氧化膜能够减缓钢铁腐蚀的原因是________;发蓝过程的化学方程式![]() ,式中X的化学式为____.为检验处理后的成品表面是否形成致密的氧化膜常往其表面滴5%硫酸铜溶液一段时间。如果氧化膜不致密(铁部分裸露出来),将观察到红色物质,试写出反应的原理_______(用化学方程式表示)
,式中X的化学式为____.为检验处理后的成品表面是否形成致密的氧化膜常往其表面滴5%硫酸铜溶液一段时间。如果氧化膜不致密(铁部分裸露出来),将观察到红色物质,试写出反应的原理_______(用化学方程式表示)
(3)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜铁质船底镶嵌的金属是________(填选项)
A Pb(铅) B Cu C Pt(铂) D Zn
【答案】单质 生成的黑色氧化膜阻碍铁与空气中的氧气与水接触 Fe3O4 Fe+CuSO4=FeSO4+Cu D
【解析】
(1)“沙里淘金”说明黄金在自然界中能够以单质形式存在,因为金的化学性质不活泼,常温下既使在高温下也很难与空气中的成分反应。
(2)钢铁零件表面上的蓝黑色氧化膜能够减缓钢铁腐蚀的原因是生成的黑色氧化膜阻碍铁与空气中的氧气与水接触,破坏了铁生锈的条件;发蓝过程中根据质量守恒定律反应前面相同元素的原子个数不变可知,反应前比反应后多36个铁原子和48个氧原子,所以12X中应含有36个铁原子和48个氧原子,即式中X的化学式为Fe3O4。
检验处理后的成品表面是否形成致密的氧化膜常往其表面滴5%硫酸铜溶液一段时间。如果氧化膜不致密(铁部分裸露出来),将观察到红色物质,是因为露出的铁会与硫酸铜反应生成硫酸亚铁和铜,即Fe+CuSO4=FeSO4+Cu。
(3)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。选项中金属适宜铁质船底镶嵌的是Zn,因为选项中只有锌的活泼性比铁强。

【题目】MgSO4和Na2CO3的溶解度表曲线如下。下列说法错误的是( )
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
溶解度S/g | MgSO4 | 25.1 | 28.2 | 30.8 | 32.9 | 34.3 | 35.0 | 34.9 |
Na2CO3 | 21.5 | 39.7 | 49.0 | 48.5 | 46.0 | 45.2 | 43.9 | |
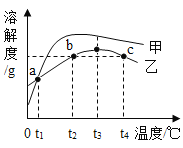
A.物质甲是 Na2CO3
B.a 点对应的温度 t1 在 20℃-30℃之间
C.a 点、b 点对应的乙的溶液,溶质质量分数一定相等
D.等质量的甲、乙溶液从 t2降温到 t1,析出晶体质量:甲一定大于乙
【题目】下列比较金属活动性强弱的实验设计、现象和结论均正确的是( )
选项 | 实验设计 | 现象 | 结论(金属的活动性) |
A | 将未经打磨的铝丝放入硫酸铜溶液中 | 无现象 |
|
B | 分别将表面积相同的镁条和铝条点燃放入盛满氧气的集气瓶中 | 铝条燃烧得更剧烈 |
|
C | 分别将锌片与铁粉放入相同浓度的稀盐酸中 | 锌片产生气泡的速率比铁粉慢 |
|
D | 分别将铁丝与铜丝放入相同浓度的稀盐酸中 | 铁丝表面产生气泡,铜丝无现象 |
|
A.AB.BC.CD.D