题目内容
【题目】已知A是绿色固体,各物质转化关系如图(部分反应物、反应条件已省略)。其中C、F、H、I是无色气体, 且C、F组成元素相同。E溶液为蓝色,I在空气中能燃烧,发出淡蓝色。回答下列问题:
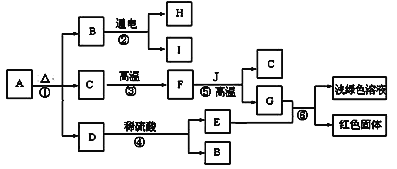
⑴A的化学式是_________,H的化学式是__________,G的化学式是__________;
⑵若J 为磁铁矿的主要成分,则反应⑤的化学方程式为___________________;
⑶反应③的化学方程式为_____________,反应⑥的化学方程式为_____________;
⑷C、F组成元素相同,但化学性质不同,其原因是_____________;
【答案】 Cu2(OH)2CO3 O2 Fe Fe3O4+4CO![]() 3Fe+4CO2 CO2+C
3Fe+4CO2 CO2+C![]() 2CO Fe+CuSO4==Cu+FeSO4 分子构成不同
2CO Fe+CuSO4==Cu+FeSO4 分子构成不同
【解析】B在通电的条件下反应,故B是水,水在通电的条件下分解生成氢气和氧气,I在空气中能燃烧,发出淡蓝色,故I是氢气,那么H是氧气;A是绿色固体,加热时能分解生成水和另外两种物质,故A是碱式碳酸铜,碱式碳酸铜分解生成氧化铜、水和二氧化碳;氧化铜能与稀硫酸反应生成硫酸铜和水,故D是氧化铜,E是硫酸铜;C、F组成元素相同,C是二氧化碳,二氧化碳和碳在高温的条件下生成一氧化碳,即F是一氧化碳;G和硫酸铜反应生成了浅绿色溶液和红色固体,浅绿色的溶液中一定含有亚铁离子,红色的固体可能是铜,故G是铁,铁和硫酸铜反应生成铜和硫酸亚铁;J 为磁铁矿的主要成分,故的四氧化三铁,一氧化碳还原四氧化三铁生成铁和二氧化碳,即J是氧化铁。把推断出的物质带入转化关系中,推断正确。(1)A是碱式碳酸铜,表示为Cu2(OH)2CO3;H是氧气,表示为O2;G是铁,表示为Fe;(2)一氧化碳还原四氧化三铁生成铁和二氧化碳,反应的化学方程式表示为Fe3O4+4CO ![]() 3Fe+4CO2;(3)反应③是二氧化碳和碳在高温的条件下生成一氧化碳,反应的化学方程式表示为CO2+C高温2CO;反应⑥是铁和硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式表示为Fe+ CuSO4 == Cu + FeSO4;(4)一氧化碳是由一氧化碳分子构成的,二氧化碳是由二氧化碳分子构成的,分构成不同,故化学性质不同。
3Fe+4CO2;(3)反应③是二氧化碳和碳在高温的条件下生成一氧化碳,反应的化学方程式表示为CO2+C高温2CO;反应⑥是铁和硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式表示为Fe+ CuSO4 == Cu + FeSO4;(4)一氧化碳是由一氧化碳分子构成的,二氧化碳是由二氧化碳分子构成的,分构成不同,故化学性质不同。

【题目】锌锰电池材料中含铜,构造如图。请回答下列问题:

⑴下列铜制品中,利用金属导电性的是_______(填字母序号);
A.铜质奖牌 B.铜导线 C.铜火锅
⑵图中所示物质属于非金属单质的化学式是_______;
⑶氯化铵中的原子团是________(填符号);
⑷金属制品在空气中放置易生锈,铁生锈的条件是_________,废旧电池铜帽会生成一些绿色的铜锈,其主要成分为是Cu2(OH)2CO3,则铜生锈还必须有________参与;
⑸普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+2MnOOH,该反应中锰元素的化合价由+4变为_________。
⑹电池铜帽为铜锌合金。某课外活动小组为测定铜帽中铜的质量分数,设计实验如下:取铜帽样品10g放入烧杯中,然后把40g稀硫酸分四次加入到烧杯中,其反应的情况如表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
剩余黄铜样品的质量/g | 8.7 | 7.4 | M | 6.6 |
①表中的M的值为__________,此黄铜样品中锌的质量分数为_________;
②从以上数据可知,这四次实验中,第_______次稀硫酸已完全反应;
③所用稀硫酸溶质的质量分数是_________?(写出解题过程)