题目内容
【题目】如图是某反应的微观示意图,关于该反应的说法中,不正确的是( ) 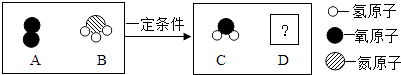
A.反应前后,原子种类、数目均不变
B.若D为单质,则A,C质量比为1:2
C.若A,B化学计量数之比为5:4,则D中含2种元素
D.该反应中,N元素的化合价一定升高
【答案】B
【解析】解:据反应的微观示意图,可以知道该反应的化学方程式是:3O2+4NH3 ![]() 6H2O+2N2 . 则 A、根据质量守恒定律,反应前后,原子种类、数目均不变,说法正确,故A正确;
6H2O+2N2 . 则 A、根据质量守恒定律,反应前后,原子种类、数目均不变,说法正确,故A正确;
B、若D为单质,则A,C质量比为(3×32):(6×18)=8:9,故B错误;
C、若A,B化学计量数之比为5:4,则可知氧气过量,故D中会有氧元素,故含2种元素,故C正确;
D、由该反应的化学方程式可知,NH3中N元素的化合价为﹣3,N2中N元素的化合价为0,故一定升高,故D正确;
故选:B.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究 . 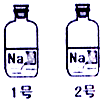
【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
实验步骤 | 实验现象 | 实验结论 |
实验1:分别测定两种溶液的pH | 两瓶溶液一定不是NaCl溶液、Na2SO4溶液 | |
实验2: | 均有气泡产生 | 两瓶溶液分别是NaHCO3溶液和Na2CO3溶液.写出Na2CO3溶液与盐酸反应的化学方程式 . |
实验3:滴加适量 | 1号溶液是Na2CO3溶液 |
【实验反思】小红经过分析认为1号溶液还可能是变质的氢氧化钠溶液,写出氢氧化钠溶液变质的化学方程式 .