题目内容
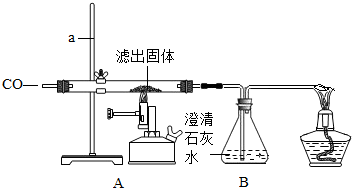
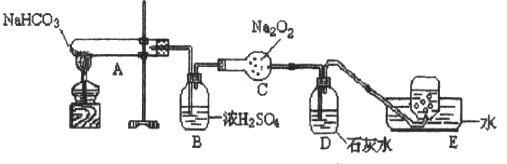
按以下装置图进行实验,填写有关现象及化学方程式

①A中现象是
②B中浓硫酸的作用是
③C中发生反应的化学方程式为
④D中现象是
⑤E中收集的气体是

①A中现象是
试管内壁有水珠
试管内壁有水珠
;②B中浓硫酸的作用是
吸收生成的水
吸收生成的水
;③C中发生反应的化学方程式为
2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
;④D中现象是
变浑浊
变浑浊
,反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
;⑤E中收集的气体是
O2
O2
.分析:①根据碳酸氢钠受热分解生成水解答;
②根据浓硫酸具有吸水性能做干燥剂解答;
③根据二氧化碳和过氧化钠反应生成碳酸钠和氧气书写;
④根据碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙和水解答;
⑤根据二氧化碳和过氧化钠反应生成氧气,氧气中的二氧化碳被D中的石灰水吸收解答.
②根据浓硫酸具有吸水性能做干燥剂解答;
③根据二氧化碳和过氧化钠反应生成碳酸钠和氧气书写;
④根据碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙和水解答;
⑤根据二氧化碳和过氧化钠反应生成氧气,氧气中的二氧化碳被D中的石灰水吸收解答.
解答:解:①碳酸氢钠受热分解生成水、二氧化碳和碳酸钠,试管内壁会出现小水珠;
②浓硫酸具有吸水性能做干燥剂;
③二氧化碳和过氧化钠反应生成碳酸钠和氧气;
④碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙和水;
⑤二氧化碳和过氧化钠反应生成氧气,氧气中的二氧化碳被D中的石灰水吸收所以E中收集的是氧气.
故答案:①试管内壁有水珠;②吸收生成的水;③2CO2+2Na2O2=2Na2CO3+O2;④变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O ⑤O2
②浓硫酸具有吸水性能做干燥剂;
③二氧化碳和过氧化钠反应生成碳酸钠和氧气;
④碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙和水;
⑤二氧化碳和过氧化钠反应生成氧气,氧气中的二氧化碳被D中的石灰水吸收所以E中收集的是氧气.
故答案:①试管内壁有水珠;②吸收生成的水;③2CO2+2Na2O2=2Na2CO3+O2;④变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O ⑤O2
点评:本题以实验的形式考查了碳酸氢钠的性质,注重分析能力的考查,综合性较强但难度不太大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目