题目内容
【题目】如图是Na2SO4溶液与BaCl2溶液混合反应的示意图:
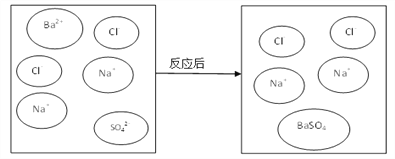
(1)发生反应时,可以观察到的现象是______________________________。
(2)溶液中还存在的一种微粒是__________(用化学用语表示,下同)。
(3)该反应的本质是___________和_______________结合成沉淀。
(4)写出与上述反应本质相同的另一化学反应方程式:______________________。
【答案】 有白色沉淀产生 H2O Ba2+ SO42- Ba(NO3)2+K2SO4===2KNO3+BaSO4
【解析】(1) Na2SO4溶液与BaCl2溶液混合反应生成硫酸钡白色沉淀和氯化钠;(2) 溶液中还存在的一种微粒是水分子;(3)根据微观示意图可知:该反应的本质是Ba2+和 SO42- 生成硫酸钡沉淀;(4) K2SO4溶液与Ba(NO3)2溶液混合反应生成硫酸钡白色沉淀和硝酸钾,反应方程式为:Ba(NO3)2+K2SO4=2KNO3+BaSO4。

 名校课堂系列答案
名校课堂系列答案【题目】某同学进行如图两个实验:

(l)甲实验中反应的化学方程式为__________________;
(2)乙实验观察到的现象是__________________;
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3。
(实验方案)
实验操作 | 实验现象与结论 |
(1)过滤、洗涤白色沉淀备用; (2)向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为___________。 ②若_________,且无气泡产生,猜想Ⅱ成立。 ③若沉淀完全溶解,________________,猜想Ⅲ成立。 |
(拓展与思考)④如果猜想Ⅲ成立,产生此结果的原因是做甲实验时__________________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是______。
【题目】将一定量的硝酸钾和氯化钠(溶解度如下表)的混合物投入适量热水中充分溶解,对该溶液进行如图所示实验(假设实验过程各物质无损耗)。
温度/℃ | 20 | 40 | 60 | 80 | 100 | |
溶解度/g |
| 31.6 | 64 | 110 | 169 | 246 |
| 35.8 | 35.4 | 37 | 38.4 | 39.8 | |

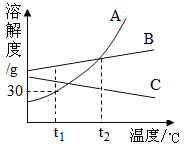
(1)上述两种物质中,____________的溶解度受温度影响较大。
(2)甲烧杯中热水的温度(t)范围为____________
(3)若将乙烧杯____________(填“趁热”或“冷却”)过滤,可获得更多量晶体。
(4)丙烧杯中的溶液为________________________的饱和溶液.
(5)![]() 时,若仅析出氯化钠晶体,则蒸发去水的质量最多不超过____________g(结果保留整数位)。
时,若仅析出氯化钠晶体,则蒸发去水的质量最多不超过____________g(结果保留整数位)。