题目内容
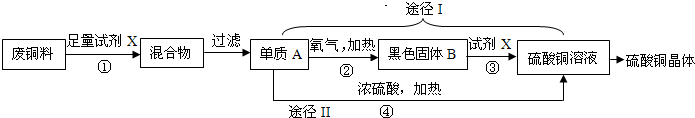
硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程.

(1)B的化学式为
(2)反应①、③的化学方程式分别为 ①
(3)已知:Cu+2H2SO4 (浓)
CuSO4+SO2↑+2H2O.从经济和环保的角度分析,对比途径I、Ⅱ,途径I的优点有:获得等量硫酸铜消耗的硫酸少和

(1)B的化学式为
CuO
CuO
,操作a的名称是过滤
过滤
.(2)反应①、③的化学方程式分别为 ①
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
; ③CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.(3)已知:Cu+2H2SO4 (浓)
| ||
减少污染
减少污染
.分析:(1)根据流程图可推断,黑色固体B应是铜在加热条件下与氧气反应的产物;单质A为不与试剂X稀硫酸反应的铜,因此,操作a是把不溶性固体和溶液分离开的操作;
(2)根据反应①为使用稀硫酸把铁反应而除去的置换反应;反应③则应是黑色固体氧化铜与稀硫酸得到硫酸而发生的复分解反应进行解答;
(3)途径II中产生二氧化硫气体不但会产生污染,而且会使部分硫酸因转化成二氧化硫而造成转化率不高.
(2)根据反应①为使用稀硫酸把铁反应而除去的置换反应;反应③则应是黑色固体氧化铜与稀硫酸得到硫酸而发生的复分解反应进行解答;
(3)途径II中产生二氧化硫气体不但会产生污染,而且会使部分硫酸因转化成二氧化硫而造成转化率不高.
解答:解:
(1)黑色固体为金属铜在加热条件下与氧气化合产生的氧化铜;操作a为过滤操作,把不与稀硫酸反应的金属铜与硫酸亚铁溶液分离开来;
故答案为:CuO;过滤;
(2)反应①则是铁与稀核酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水,化学方程式为CuO+H2SO4=CuSO4+H2O;
故答案为:Fe+H2SO4=FeSO4+H2↑;CuO+H2SO4=CuSO4+H2O;
(3)途径II中产生二氧化硫气体不但会产生污染,而且会使部分硫酸因转化成二氧化硫而造成转化率不高,所以对比途径I、Ⅱ,途径I的优点有:获得等量硫酸铜消耗的硫酸少和减少污染;
故答案为:减少污染.
(1)黑色固体为金属铜在加热条件下与氧气化合产生的氧化铜;操作a为过滤操作,把不与稀硫酸反应的金属铜与硫酸亚铁溶液分离开来;
故答案为:CuO;过滤;
(2)反应①则是铁与稀核酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水,化学方程式为CuO+H2SO4=CuSO4+H2O;
故答案为:Fe+H2SO4=FeSO4+H2↑;CuO+H2SO4=CuSO4+H2O;
(3)途径II中产生二氧化硫气体不但会产生污染,而且会使部分硫酸因转化成二氧化硫而造成转化率不高,所以对比途径I、Ⅱ,途径I的优点有:获得等量硫酸铜消耗的硫酸少和减少污染;
故答案为:减少污染.
点评:根据生产流程图,正确理解每个过程在生产中的作用,从而达到全面掌握生产过程的目的,为解答问题做足准备.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目