题目内容
25、常温下,氨气是一种具有刺激性气味的气体,极易溶于水,生成的NH3?H2O能够解离出OH-使氨水呈碱性.
(1)请书写氨气的化学式:
(2)已知20℃时氨气的溶解度为700.“700”的含义是
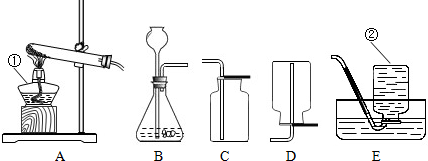
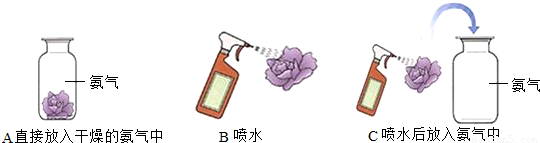
(3)取三朵用紫色石蕊试液染色的干燥的纸花,分别做A、B、C三个实验(如图所示).

①请描述A、B、C三个实验的现象:
②请回答C中水的作用:
(1)请书写氨气的化学式:
NH3
.(2)已知20℃时氨气的溶解度为700.“700”的含义是
压强为101kPa和温度为20℃时,1体积水中溶解700体积氨气时溶液达到饱和
.(3)取三朵用紫色石蕊试液染色的干燥的纸花,分别做A、B、C三个实验(如图所示).

①请描述A、B、C三个实验的现象:
A和B中的纸花都没变色,C中的纸花会变成蓝色
;②请回答C中水的作用:
水与氨气反应生成NH3?H2O,NH3?H2O在水中会解离出OH-
.分析:抓住某些物质的性质:氨气不呈碱性,紫色石蕊试液只有遇到碱性溶液才能变蓝.气体的溶解度是指某温度下,一体积水中最多溶解的这种气体的体积,和固体溶解度的概念不一样.
解答:解:(1)每个氨气分子是由一个氮原子和三个氢原子构成的,故答案为:NH3
(2)气体的溶解度指的是在压强为101kPa,某温度下,一体积水中最多溶解的这种气体的体积.故答案为:在压强为101kPa和温度为20℃时,1体积水中溶解700体积氨气时溶液达到饱和
(3)由于氨气和水都不具有碱性的,因此都不能使纸花变色,而氨气能和水发生反应生成NH3?H2O,能电离出氢氧根离子,从而使氨水显碱性,故答案为:①A与B的纸花不变色,C的纸花变蓝色
②水与氨气反应生成NH3?H2O,NH3?H2O在水中会解离出OH-
(2)气体的溶解度指的是在压强为101kPa,某温度下,一体积水中最多溶解的这种气体的体积.故答案为:在压强为101kPa和温度为20℃时,1体积水中溶解700体积氨气时溶液达到饱和
(3)由于氨气和水都不具有碱性的,因此都不能使纸花变色,而氨气能和水发生反应生成NH3?H2O,能电离出氢氧根离子,从而使氨水显碱性,故答案为:①A与B的纸花不变色,C的纸花变蓝色
②水与氨气反应生成NH3?H2O,NH3?H2O在水中会解离出OH-
点评:主要探究了氨气的性质,培养学生分析问题、解决问题的能力和总结知识的能力.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目