题目内容
【题目】张南同学和小岗同学以探究锌、铁、铜三种金属的活动性为课题,进行科学探究活 动,请根据已学知识完成下列问题。
(提出问题)锌、铁、铜的金属活动性顺序是怎样的?
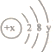
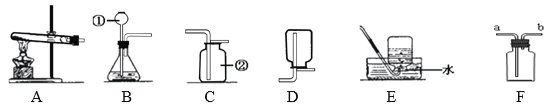
(制订计划)张南同学、小岗同学设计的实验(一次性探究)如图所示,张南实验的烧杯中盛有一种酸溶液,小岗实验的烧杯中盛有一种硝酸盐溶液。他们在实验中都进行了规范的操作和细致的观察,通过实验他们都得出了正确的结论。
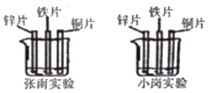
(收集证据)你认为张南同学的实验中应观察到的现象是
(1)__________。
(2)由此得出三种金属的活动性顺序是_________。
(3)(解释与结论)小岗同学的实验中发生反应的化学方程式为_____________;
(4)实验后小岗同学烧杯中溶液一定含有的离子有___________。
【答案】银白色的锌片反应的比较剧烈,表面有大量气泡产生,银白色的铁片反应的比较缓慢,表面有少量气泡产生,紫红色铜片表面无明显现象; Zn>Fe>Cu; Zn+ Fe(NO3)2= Fe+ Zn(NO3)2; Zn2+、![]()
【解析】
(1)实验中张南同学应观察到的现象是:银白色的锌片反应的比较剧烈,表面有大量气泡产生,银白色的铁片反应的比较缓慢,表面有少量气泡产生,紫红色铜片表面无明显现象;
(2)由实验现象可得出三种金属的活动性顺序是:Zn>Fe>Cu;
(3)【解释与结论】锌与硝酸亚铁溶液反应生成铁和硝酸锌,发生反应的化学方程式为:Zn+ Fe(NO3)2= Fe+ Zn(NO3)2;
(4)锌与硝酸亚铁溶液反应生成铁和硝酸锌,所以溶液中一定含有的离子有:Zn2+、![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】途运输鱼苗时,常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙的时产生气泡。
(査阅资料)氢氧化钙的水溶液就是石灰水。
(提出问题)当把过氧化钙投入足量水中时,最终生成什么物质?
(进行猜想)甲同学:生成碳酸和氧气;
乙同学:生成氢氧化钙和氧气。
同学和老师都认为甲同学的猜想是错误的,其理由是________。
(实验探究)
(1)打开下图装置中分液漏斗的活塞,控制滴加水速度,观察到试管内有气泡产生。
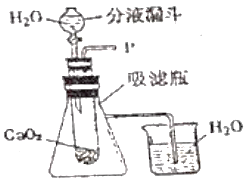
①___________(填实验操作),说明生成的气体是氧气。
②实验过程中,发现烧杯中有气泡出现,该现象说明___________。
(2)请设计一个实验方案来验证过氧化钙和水反应产生的另一种物质是氢氧化钙:
实验步骤及操作方法 | 预期的实验现象 | 结论 |
①取少量过氧化钙放入试管中,加足量水,震荡,②往所得溶液中通入____________。 | ①产生气泡, ②_________。 | 过氧化钙和水反应产生的另一种物质是氢氧化钙 |
(问题讨论)
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是________;
(2)过氧化钙和水反应的化学方程式为____________。