题目内容
24、下表中所列是元素周期表中部分元素的原子结构示意图、主要化合价等信息.
(1)从原子结构看,Na和Mg同属于第三周期的原因是
(2)从元素种类看,每一周期从左到右由
(3)请写出原子序数为8和14的元素所组成化合物的化学式:

(1)从原子结构看,Na和Mg同属于第三周期的原因是
电子层数都为3
,F和Cl同属于ⅦA(读作“第七主族”)的原因是最外层电子数都为7
.(2)从元素种类看,每一周期从左到右由
金属
元素过渡到非金属
元素,并以稀有气体元素结尾.(3)请写出原子序数为8和14的元素所组成化合物的化学式:
SiO2
.分析:根据元素周期律:周期数与该原子的电子层数相同,族数值与该原子的最外层电子数相同,元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束,进行分析解答本题.
解答:答:(1)根据元素周期律,元素所在周期数与该原子电子层数相同,从原子结构看,Na和Mg同属于第三周期的原因是电子层数都是3;根据元素周期律族数值与该原子的最外层电子数相同,F和Cl同属于ⅦA(读作“第七主族”)的原因是最外层电子数都为7;
故答案为:电子层数都为3;最外层电子数都为7;
(2)根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始).在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)和元素性质,也发生规律性的变化.
故答案为:金属;非金属;
(3)从元素周期表中可查出原子序数为8和14的元素分别为 O,Si,所组成化合物的化学式为:SiO2,
故答案为:SiO2.
故答案为:电子层数都为3;最外层电子数都为7;
(2)根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始).在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)和元素性质,也发生规律性的变化.
故答案为:金属;非金属;
(3)从元素周期表中可查出原子序数为8和14的元素分别为 O,Si,所组成化合物的化学式为:SiO2,
故答案为:SiO2.
点评:本题考查学生对元素周期表知识的综合应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2009?白下区二模)下表中所列是元素周期表中部分元素的原子结构示意图、主要化合价等信息.
(1)从原子结构看,Na和Mg同属于第三周期的原因是______,F和Cl同属于ⅦA(读作“第七主族”)的原因是______.
(2)从元素种类看,每一周期从左到右由______元素过渡到______元素,并以稀有气体元素结尾.
(3)请写出原子序数为8和14的元素所组成化合物的化学式:______.
| 第二周期 |  Li Li |  Be |  B |  C |  N |  O O |  F |
| 主要化合价 | +1 | +2 | +3 | +4,-4 | +5,-3 | -2 | -1 |
| 第三周期 |  Na |  Mg |  Al |  Si |  P |  S | 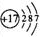 Cl |
| 主要化合价 | +1 | +2 | +3 | +4,-4 | +5,-3 | +6,-2 | +7,-1 |
(2)从元素种类看,每一周期从左到右由______元素过渡到______元素,并以稀有气体元素结尾.
(3)请写出原子序数为8和14的元素所组成化合物的化学式:______.


