题目内容
(1)为了验证烧碱样品中是否含有氯化钠,正确的操作步骤是;
①______;②______;③______.
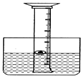
(2)如图,为了研究空气中所含氧气的体积,用一个50mL量筒倒扣在水中,量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有少量白磷.现把氢氧化钠缓缓投入水中并搅拌,这样做的原因是______.放白磷的小船用铜做的原因是______.一会儿,白磷发生自燃,观察到______,最终,液面大约位于量筒刻度______处.
(3)金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色.某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了.
据你推测,导致溶液碱性变化的原因是:
①______;
②______.
请设计一个实验来验证你的一种推测,简要说明操作、现象及结论.______.
①______;②______;③______.
(2)如图,为了研究空气中所含氧气的体积,用一个50mL量筒倒扣在水中,量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有少量白磷.现把氢氧化钠缓缓投入水中并搅拌,这样做的原因是______.放白磷的小船用铜做的原因是______.一会儿,白磷发生自燃,观察到______,最终,液面大约位于量筒刻度______处.
(3)金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色.某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气中一段时间后,发现溶液的红色褪去了.
据你推测,导致溶液碱性变化的原因是:
①______;
②______.
请设计一个实验来验证你的一种推测,简要说明操作、现象及结论.______.

(1)①配置溶液:用蒸馏水将烧碱样品溶解、配成溶液;
②除去OH-离子:加入硝酸使溶液的pH<7(用pH试纸试验);
③验证Cl-的存在:加入硝酸银溶液,若有白色沉淀生成证明有NaCl存在,反之就没有NaCl存在.
故答案是:①用蒸馏水将烧碱样品溶解、配成溶液;②加入硝酸使溶液的pH<7(用pH试纸试验);③加入硝酸银溶液,若有白色沉淀生成证明有NaCl存在,反之就没有NaCl存在.
(2)氢氧化钠溶于水放出热量,使溶液温度升高,从而达到白磷的着火点让白磷燃烧.盛放白磷的容器要有很好的导热性,故放白磷的小船用铜做的原因是:铜导热性好且化学性质稳定.磷燃烧生成五氧化二磷固体产生浓厚的白烟;磷燃烧消耗氧气,生成五氧化二磷固体,量筒内气压减小,小船中的水上升.氧气约占空气体积的1/5,故水应上升到32mL处;
故答案为:NaOH固体溶解于水时放出热量,使溶液温度升高,达到白磷的着火点;产生大量白烟,量筒内液面上升;32mL.
(3)根据金属镁可与热水反应生成一种碱和一种气体,滴加酚酞试液,溶液变为红色的信息,我们可以大胆的猜测,这种碱可能是氢氧化镁.放置在空气中冷却后,发现溶液的红色褪去了,根据碱能与二氧化碳反应的化学性质,或者我们很容易会想到是否是碱性溶液与空气中的二氧化碳反应生成了其他的盐;根据氢氧化镁微溶于水的性质和物质的溶解度受温度的影响,我们可以猜测温度降低,Mg(OH)2溶解度变小了;根据氢氧化镁微溶于水的性质和物质的溶解度受温度的影响,我们可以猜测温度降低,Mg(OH)2溶解度变小了,从而设计加热褪色的溶液,观察溶液颜色变化的实验;
故答案为:①氢氧化镁的溶解度随着温度的降低而减小,从而使溶液碱性消失(或减弱);②吸收了空气中的二氧化碳而使溶液碱性消失(或减弱).
将褪色后的溶液再加热,看其是否再变为红色,如变红,则原因为①.(或将溶液在隔绝空气的条件下降温,看其红色是否褪去.如不褪去,则原因为②).
②除去OH-离子:加入硝酸使溶液的pH<7(用pH试纸试验);
③验证Cl-的存在:加入硝酸银溶液,若有白色沉淀生成证明有NaCl存在,反之就没有NaCl存在.
故答案是:①用蒸馏水将烧碱样品溶解、配成溶液;②加入硝酸使溶液的pH<7(用pH试纸试验);③加入硝酸银溶液,若有白色沉淀生成证明有NaCl存在,反之就没有NaCl存在.
(2)氢氧化钠溶于水放出热量,使溶液温度升高,从而达到白磷的着火点让白磷燃烧.盛放白磷的容器要有很好的导热性,故放白磷的小船用铜做的原因是:铜导热性好且化学性质稳定.磷燃烧生成五氧化二磷固体产生浓厚的白烟;磷燃烧消耗氧气,生成五氧化二磷固体,量筒内气压减小,小船中的水上升.氧气约占空气体积的1/5,故水应上升到32mL处;
故答案为:NaOH固体溶解于水时放出热量,使溶液温度升高,达到白磷的着火点;产生大量白烟,量筒内液面上升;32mL.
(3)根据金属镁可与热水反应生成一种碱和一种气体,滴加酚酞试液,溶液变为红色的信息,我们可以大胆的猜测,这种碱可能是氢氧化镁.放置在空气中冷却后,发现溶液的红色褪去了,根据碱能与二氧化碳反应的化学性质,或者我们很容易会想到是否是碱性溶液与空气中的二氧化碳反应生成了其他的盐;根据氢氧化镁微溶于水的性质和物质的溶解度受温度的影响,我们可以猜测温度降低,Mg(OH)2溶解度变小了;根据氢氧化镁微溶于水的性质和物质的溶解度受温度的影响,我们可以猜测温度降低,Mg(OH)2溶解度变小了,从而设计加热褪色的溶液,观察溶液颜色变化的实验;
故答案为:①氢氧化镁的溶解度随着温度的降低而减小,从而使溶液碱性消失(或减弱);②吸收了空气中的二氧化碳而使溶液碱性消失(或减弱).
将褪色后的溶液再加热,看其是否再变为红色,如变红,则原因为①.(或将溶液在隔绝空气的条件下降温,看其红色是否褪去.如不褪去,则原因为②).

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目


