题目内容
天然气的主要成分是甲烷(CH4),其燃烧会产生二氧化碳和水,反应过程为:CH4+2O2 CO2+H2O,请计算:
CO2+H2O,请计算:(1)甲烷的相对分子质量______.
(2)甲烷中碳氢元素的质量比______.
(3)1.6g甲烷中含有______碳元素.
(4)1.6g甲烷充分燃烧后,能生成二氧化碳______g.
【答案】分析:(1)根据相对分子质量等于各原子的相对原子质量之和解答;
(2)根据化合物中各元素的质量比等于各原子的相对原子质量之和的比解答;
(3)根据甲烷中碳元素的质量分数和甲烷的质量解答;
(4)根据反应化学方程式为:CH4+2O2 CO2+H2O,利用甲烷的质量求出二氧化碳的质量.
CO2+H2O,利用甲烷的质量求出二氧化碳的质量.
解答:解:(1)由甲烷的化学式的CH4,相对分子质量=12+1×4=16;
(2)甲烷中碳、氢元素的质量比=12:(1×4)=3:1;
(3)甲烷中碳元素的质量分数和甲烷的质量,则1.6g×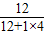 ×100%=1.2g
×100%=1.2g
答:1.6g甲烷中含有1.2g碳元素;
(4)设生成二氧化碳的质量为x.
CH4+2O2 CO2+H2O
CO2+H2O
16 44
1.6g x
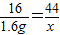
x=4.4g
答:生成二氧化碳的质量为4.4g.
故答案为:(1)16;(2)1:3;(3)1.2g;(4)4.4g.
点评:化学式可以表示物质的组成和构成,根据物质的化学式可进行相对分子质量、组成元素的质量比、组成元素的质量分数等计算以及有关化学方程式的计算.
(2)根据化合物中各元素的质量比等于各原子的相对原子质量之和的比解答;
(3)根据甲烷中碳元素的质量分数和甲烷的质量解答;
(4)根据反应化学方程式为:CH4+2O2
 CO2+H2O,利用甲烷的质量求出二氧化碳的质量.
CO2+H2O,利用甲烷的质量求出二氧化碳的质量.解答:解:(1)由甲烷的化学式的CH4,相对分子质量=12+1×4=16;
(2)甲烷中碳、氢元素的质量比=12:(1×4)=3:1;
(3)甲烷中碳元素的质量分数和甲烷的质量,则1.6g×
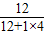 ×100%=1.2g
×100%=1.2g答:1.6g甲烷中含有1.2g碳元素;
(4)设生成二氧化碳的质量为x.
CH4+2O2
 CO2+H2O
CO2+H2O16 44
1.6g x
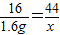
x=4.4g
答:生成二氧化碳的质量为4.4g.
故答案为:(1)16;(2)1:3;(3)1.2g;(4)4.4g.
点评:化学式可以表示物质的组成和构成,根据物质的化学式可进行相对分子质量、组成元素的质量比、组成元素的质量分数等计算以及有关化学方程式的计算.

练习册系列答案
相关题目
 B.
B. C.
C. D.
D.