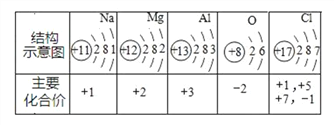
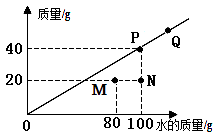
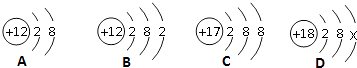��Ŀ����
����Ŀ��һ��������Һ�����ܺ���H+��Na+��Ba2+��Fe3+��Cl-��OH-��SO42-���ӵ�һ�ֻ��֡�Ϊȷ����Һ�п��ܴ��ڵ����ӣ���������ʵ�顣
�پ��ⶨ����Һ��pH=1��
��ȡ������Ʒ�μ�NaOH��Һ���г������ɡ������μ�NaOH��Һ�����ٲ�������Ϊֹ�����ˣ�
����ʵ��ڵõ�����Һ�м����μ�Na2CO3��Һ���ֹ۲쵽��������.����ʵ��õ������½����У���ȷ����( )��
A.��Һ��һ������H+��Ba2+��Cl- �� һ��������Na+��Fe3+��OH-��SO42-
B.��Һ��һ������H+��Ba2+��Fe3+��Cl- �� һ��������Na+��OH-��SO42-
C.��Һ��һ������H+��Ba2+��Fe3+��Cl- �� һ��������OH-��SO42- �� ���ܺ���Na+
D.��Һ��һ������H+��Ba2+��Na+��Fe3+ �� һ��������OH-��SO42- �� ���ܺ���Cl-
���𰸡�C
���������پ��ⶨ����Һ��pH=1������Һ�����ԣ�һ������H+��һ��������OH������ȡ������Ʒ��Һ�μ�NaOH��Һ���г������ɣ�һ����Fe3+������ʵ��ڵõ�����Һ�еμ�Na2CO3��Һ���ֹ۲쵽�������ɣ�֤����Һ�к���Ba2+ �� ��һ��������SO ![]() ����Һ����������ƽ�⣬����һ������Cl����������������Һ��һ������H+��Ba2+��Fe3+��Cl�� �� һ��������OH����SO
����Һ����������ƽ�⣬����һ������Cl����������������Һ��һ������H+��Ba2+��Fe3+��Cl�� �� һ��������OH����SO ![]() �����ܺ���Na+ �� C�������⡣
�����ܺ���Na+ �� C�������⡣
�ʴ�Ϊ��C��������Ҫ�������ӵļ�����Ҫ��������֮�䷴Ӧ����������жϡ�

����Ŀ����Ӣͬѧȡij��ʯ��ʯ��Ʒ12g���вⶨʵ�飬�ֽ�100gϡ�������μ���ʯ��ʯ��Ʒ��(���ʲ�����ˮҲ�����뷴Ӧ)����ַ�Ӧ����������������������±���ʾ��
����ϡ���������/g | ���������������/g | |
��1�� | 20 | 1.1 |
��2�� | 20 | 2.2 |
��3�� | 20 | m |
��4�� | 20 | 4.4 |
��5�� | 20 | 4.4 |
(1)m��ֵΪ_________g
(2)12gʯ��ʯ��Ʒ��̼��Ƶ���������_________g
(3)��Ӧ��ȫ��������Һ���Ȼ��Ƶ���������Ϊ_______��(д��������̣���������ȷ��0.1)