题目内容
【题目】若将50g18%的NaOH溶液与50g18%的盐酸混和,下列叙述正确的是
A. 混合溶液的pH=7 B. 混合溶液中生成物的溶质质量分数仍为18%
C. 溶液混合前后的温度不变 D. 混合溶液的质量为100g
【答案】D
【解析】设50g18%的NaOH溶液与盐酸中氯化氢反应的质量 为x,生成氯化钠的质量为y。
HCl+NaOH═NaCl+H2O
36.540 58.5
x50g×18% y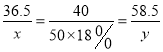
x=8.2125g
y=13.1625g
50g×18%>8.2125g,故反应后盐酸剩余,溶液显酸性。
A、50g18%的NaOH溶液与50g18%的盐酸反应后,盐酸剩余,溶液显酸性,混合溶液的pH<7,错误;B、反应后生成物的溶质质量分数为: ![]() =13.1625%,错误;C、氢氧化钠与盐酸反应放出热量,反应后溶液的温度升高,错误;D、根据质量守恒定律,反应后物质的总质量不变,混合后溶液的总质量为100g,正确。故选D。
=13.1625%,错误;C、氢氧化钠与盐酸反应放出热量,反应后溶液的温度升高,错误;D、根据质量守恒定律,反应后物质的总质量不变,混合后溶液的总质量为100g,正确。故选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目