题目内容
下列图正确的是( )
A、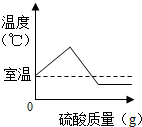 浓硫酸加入水中 浓硫酸加入水中 |
B、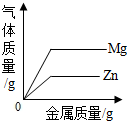 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉 |
C、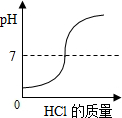 NaOH溶液中滴入稀盐酸 NaOH溶液中滴入稀盐酸 |
D、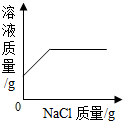 向NaCl不饱和溶液加入NaCl 向NaCl不饱和溶液加入NaCl |
考点:浓硫酸的性质及浓硫酸的稀释,饱和溶液和不饱和溶液,金属的化学性质,中和反应及其应用
专题:元素化合物知识型
分析:A、根据浓硫酸溶入水是放热反应进行判断;
B、根据氢元素的质量守恒来进行判断;
C、酸碱发生中和反应,随着反应的进行,pH值不断减小一直到pH值为7;当酸过量时,pH小于7;
D、刚开始溶液是氯化钠的不饱和溶液,则溶质氯化钠一定不是0;当不断加入氯化钠固体时,溶质的质量不断增大,溶质的质量分数逐渐增大;当氯化钠加入到一定程度,不能够再溶解,达到饱和状态,此时溶质的质量不变,溶质的质量分数不再变化.
B、根据氢元素的质量守恒来进行判断;
C、酸碱发生中和反应,随着反应的进行,pH值不断减小一直到pH值为7;当酸过量时,pH小于7;
D、刚开始溶液是氯化钠的不饱和溶液,则溶质氯化钠一定不是0;当不断加入氯化钠固体时,溶质的质量不断增大,溶质的质量分数逐渐增大;当氯化钠加入到一定程度,不能够再溶解,达到饱和状态,此时溶质的质量不变,溶质的质量分数不再变化.
解答:解:A、浓硫酸溶于水中会放出大量的热,所以室温会不断升高,随着浓硫酸质量的增加,该溶液达到饱和状态,所以温度不再改变.故A错误;
B、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,图中信息可知,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故B错误;
C、向NaOH溶液中滴入稀盐酸,一开始碱过量,pH大于7,随着反应的进行,pH值不断减小一直到pH值等于7;当酸过量时,pH小于7.故C错误;
D、刚开始是不饱和NaCl溶液,溶质NaCl的质量大于0;当不断加入NaCl固体时,溶质的质量在不断增加,溶质的质量分数逐渐增大;当NaCl不再溶解时,溶液饱和,溶质不变,溶质的质量分数也恒定不变.故D正确.
故选:D.
B、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,图中信息可知,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故B错误;
C、向NaOH溶液中滴入稀盐酸,一开始碱过量,pH大于7,随着反应的进行,pH值不断减小一直到pH值等于7;当酸过量时,pH小于7.故C错误;
D、刚开始是不饱和NaCl溶液,溶质NaCl的质量大于0;当不断加入NaCl固体时,溶质的质量在不断增加,溶质的质量分数逐渐增大;当NaCl不再溶解时,溶液饱和,溶质不变,溶质的质量分数也恒定不变.故D正确.
故选:D.
点评:本题运用图象的形式考查了浓硫酸的稀释、中和反应、金属与酸的反应、饱和溶液、不饱和溶液与溶液的质量分数之间的关系,用函数图象更能形象直观简洁地表示一些化学现象,通过图象的培养学生分析能力.

练习册系列答案
相关题目
有两瓶无色无味的气体,分别是氧气和二氧化碳,下列方法不能区别它们的是( )
| A、用燃着的木条分别试之 |
| B、用澄清石灰水分别试之 |
| C、用带火星的木条分别试之 |
| D、闻气味 |
下列有关铁的叙述中错误的是( )
| A、生铁是含杂质很多的铁合金 |
| B、不锈钢所含主要元素有Fe、Cr、C、Ni等 |
| C、铁能跟盐酸发生置换反应 |
| D、铁是构成血红蛋白的成分之一 |
下列操作正确的是( )
| A、实验完毕迅速的用嘴吹灭酒精灯 |
| B、给液体加热时试管口不对着自己或别人 |
| C、加热试管里固体时试管破裂与试管口向上倾斜无关 |
| D、试管夹一般夹在试管的中下部 |
不能用酸和金属直接反应得到的是( )
| A、FeCl2 |
| B、FeCl3 |
| C、MgSO4 |
| D、MgCl2 |
将金属Cu投入金属A的盐溶液中,观察到Cu的表面出现银白色物质;金属B投入稀硫酸中,观察到B的表面有气泡产生.下列关于金属A、B、Cu活动性的叙述正确的是( )
| A、B>A>Cu |
| B、A>Cu>B |
| C、B>Cu>A |
| D、A>B>Cu |
下列四个图象中,能正确表示反应对应变化关系的是( )
A、 向一定量的氢氧化钠溶液中滴加稀盐酸 |
B、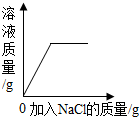 一定温度下,不饱和氯化钠溶液中加入氯化钠固体 |
C、 室温时,向一定量的稀盐酸中加入少量镁条 |
D、 用等质量、等浓度的双氧水分别制取氧气 |
下列物质在盛氧气的集气瓶中燃烧时,集气瓶底需预先铺上一薄层细沙或少量水的是( )
①木炭 ②铝箔 ③硫磺 ④铁丝 ⑤红磷.
①木炭 ②铝箔 ③硫磺 ④铁丝 ⑤红磷.
| A、①② | B、②④ | C、②⑤ | D、③⑤ |