��Ŀ����
��̼����������ָͨ��һ���ķ���������ҵ�����в�����CO2����������д������ �á���������NaOH��Һ������CO2������̵�ʾ��ͼ���£���������������δ�������

�����йظù��̵�������ȷ����
A.�ù��̿�ʵ�� CO2 ���ŷ�
B.���������У����ٷ����� 4 ����ѧ��Ӧ
C.���������У�ֻ�� 1 �����ʿ���ѭ������
D.����Ӧ�����롱�Ĺ����У��������ʵIJ������������ᾧ
�ҹ��Ŵ���֯ҵ������ľ�ң���Ҫ�ɷ�K2CO3������ʯ����ˮ�л�ϣ����ϲ���ҺƯ��֯�
�����ϣ���K2CO3 + Ca(OH)2 = CaCO3�� + 2KOH
��Ca(OH)2��K2CO3 �� KOH �IJ����ܽ�����±���
�¶�/�� | 0 | 10 | 20 | 30 | 50 | |
�ܽ��/g | Ca(OH)2 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 |
K2CO3 | 107 | 109 | 110 | 114 | 121 | |
KOH | 97 | 103 | 112 | 126 | 140 |
��1��20��ʱ��100 g ˮ�������ܽ� K2CO3 ��������__________g�����ʵ���������Ϊ 50% �� KOH ��Һ���� ___________��Һ������͡������͡�����
��2��ij�¶�ʱ����һ�����ı�������������Һ�м���������ʯ�ң��ָ���ԭ�¶ȣ�ijЩ����ʱ��仯�Ĺ�ϵ��ͼ��ʾ������������ܱ�ʾ����____________������ţ�
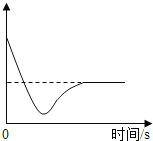
a���ʵ����� b���ʵ��������� c �������Ƶ��ܽ�� d�ܼ������� e��Һ������
��3��20��ʱ���� 1.38 g K2CO3 ������� 100 g ˮ�У�������һ�������������ƣ�����ʹ���ַ�Ӧ���ָ���ԭ�¶ȣ����ˣ��õ�����Ϊ 1.5 g �Ĺ��塣������Һ�е�������____________�������������Ƶ�������_________g��
��4�����������Ȼ������Ƴ���Һ��20��ʱ���� 4 ��ʢ�� 200 g ˮ���ձ��У��ֱ����һ���������Ȼ��Ʋ�����ܽ⡣4 ��ʵ���������£�
ʵ����� | �� | �� | �� | �� |
�����Ȼ��Ƶ�������g | 9 | 36 | 81 | 90 |
��Һ������g | 209 | 236 | 272 | 272 |
�������еõ�����Һϡ�ͳ���������Ϊ 0.9%��������ˮ�����ˮ��������________g����������ʵ���������ȷ����__________������ţ���
a�٢�������Һ�Dz�������Һ
b�ۢ�������Һ�У����ʵ������������
c20��ʱ��200 g ˮ������ܽ��Ȼ��Ƶ�����Ϊ 72 g
d20��ʱ�����ܼ����������� 100 g ˮ�����ˣ��õ�����Ϊ 36 g �Ĺ���
�뽫�������ʺͶ�Ӧ����;����_____��
���� ��; |
�ɱ� ��ζƷ ����̿ ����� ʳ�� ȥ����ζ |



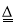 Cu + H2O B.2Mg + CO2
Cu + H2O B.2Mg + CO2  2MgO + C
2MgO + C