题目内容
维生素C(化学式为C6H8O6)对人体皮肤和牙龈的健康有重要作用,缺乏维生素C会引起坏血病.经研究表明,青少年每天都需要摄入60mg的维生素C,其中12mg由水果补充.(除不尽,结果保留一位小数)
请计算:(1)维生素C的相对分子质量为______;
(2)维生素C中各元素的质量比为______;
(3)维生素C中氧元素的质量分数是多少?
(4)若食用的水果以苹果计,已知每100g苹果含有维生素C的质量为4mg,那么每天需吃苹果的质量是多少克?
解:(1)维生素C(化学式为C6H8O6)的相对分子质量=12×6+1×8+16×6=176.
(2)根据维生素C(化学式为C6H8O)可知,维生素C中碳、氢、氧三种元素的质量比=(12×6):(1×8):(16×6)=9:1:12.
(3)维生素C中碳元素的质量分数= 100%=54.5%.
100%=54.5%.
(4)根据题意知青少年每天需要从水果中摄取12mg维生素,已知100g苹果中含维生素4mg,所以需要吃苹果300g,就会摄取到12mg维生素.
故答案为:(1)176;(2)9:1:12;(3)54.5%;(4)300g.
分析:(1)化学式中相对分子质量等于各元素相对原子质量之和,据此进行计算即可.
(2)根据元素的质量比等于原子个数乘以相对原子质量进行计算.
(3)元素的质量分数=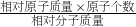 ×100%.
×100%.
(4)根据每天需要从水果中摄入的维生素的质量,再结合每100g苹果中维生素含量进行简单计算即可.
点评:本题难度不大,考查同学们新信息处理、灵活运用所学化学式的有关计算进行分析问题、解决问题的能力.
(2)根据维生素C(化学式为C6H8O)可知,维生素C中碳、氢、氧三种元素的质量比=(12×6):(1×8):(16×6)=9:1:12.
(3)维生素C中碳元素的质量分数=
 100%=54.5%.
100%=54.5%.(4)根据题意知青少年每天需要从水果中摄取12mg维生素,已知100g苹果中含维生素4mg,所以需要吃苹果300g,就会摄取到12mg维生素.
故答案为:(1)176;(2)9:1:12;(3)54.5%;(4)300g.
分析:(1)化学式中相对分子质量等于各元素相对原子质量之和,据此进行计算即可.
(2)根据元素的质量比等于原子个数乘以相对原子质量进行计算.
(3)元素的质量分数=
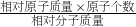 ×100%.
×100%.(4)根据每天需要从水果中摄入的维生素的质量,再结合每100g苹果中维生素含量进行简单计算即可.
点评:本题难度不大,考查同学们新信息处理、灵活运用所学化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
维生素是人体需要的一种营养素,可以提高抵抗力.已知维生素C的化学式为C6H8O6,则下列说法不正确的是( )
| A、维生素C含有碳、氢、氧三种元素 | B、维生素C是化合物 | C、维生素C中三种元素的原子个数比为6:8:6 | D、维生素C是由碳原子、氧原子、氢原子构成的 |
 九年级小伟同学体检时得知缺维生素C(化学式为C6H8O6),校医开了一瓶维生素C,请小伟同学按说明书要求服用,五天一个“疗程”.
九年级小伟同学体检时得知缺维生素C(化学式为C6H8O6),校医开了一瓶维生素C,请小伟同学按说明书要求服用,五天一个“疗程”.