题目内容
偏二甲肼是火箭推进器的常用燃料,其化学式是C2H8N2,试计算:(要求写出计算过程,否则不计分)
(1)该物质中碳元素与氢元素质量比为
(2)该物质中碳元素的质量分数为
(3)120g该物质中含氮元素的质量为
(4)相同质量的C2H8N2与C6H12O6(葡萄糖)中所含碳元素的质量比为
(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,则混合物中氢元素的质量为
(1)该物质中碳元素与氢元素质量比为
3:1
3:1
;(2)该物质中碳元素的质量分数为
40%
40%
;(3)120g该物质中含氮元素的质量为
56g
56g
;(4)相同质量的C2H8N2与C6H12O6(葡萄糖)中所含碳元素的质量比为
1:1
1:1
;(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,则混合物中氢元素的质量为
6g
6g
.分析:(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=
×100%,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,可计算出混合物中C2H8N2的质量,进而可计算出C2H8N2中含有碳元素和氢元素的质量、C3H8中含碳元素的质量,最后可计算出氢元素的质量.
(2)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,可计算出混合物中C2H8N2的质量,进而可计算出C2H8N2中含有碳元素和氢元素的质量、C3H8中含碳元素的质量,最后可计算出氢元素的质量.
解答:解:(1)该物质中碳元素与氢元素质量比为(12×2):(1×8)=3:1.
(2)该物质中碳元素的质量分数为
×100%=40%.
(3)120g该物质中含氮元素的质量为120g×
×100%=56g.
(4)设它们的质量均为m,则相同质量的C2H8N2与C6H12O6(葡萄糖)中所含碳元素的质量比为(m×40%):(m×
×100%)=1:1.
(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,则混合物中C2H8N2的质量为14g÷(
×100%)=30g,C2H8N2中含有碳元素的质量为30g×40%=12g;则C2H8N2中含有氢元素的质量为30g-14g-12g=4g;C3H8中含碳元素的质量为21g-12g=9g,含氢元素的质量为
×9g=2g;则则混合物中氢元素的质量为4g+2g=6g.
故答案为:(1)3:1;(2)40;(3)56g;(4)1:1;(5)6g.
(2)该物质中碳元素的质量分数为
| 12×2 |
| 12×2+1×8+14×2 |
(3)120g该物质中含氮元素的质量为120g×
| 14×2 |
| 12×2+1×8+14×2 |
(4)设它们的质量均为m,则相同质量的C2H8N2与C6H12O6(葡萄糖)中所含碳元素的质量比为(m×40%):(m×
| 12×6 |
| 12×6+1×12+16×6 |
(5)由C2H8N2与C3H8组成的混合物中,所含碳元素的质量21g,氮元素的质量14g,则混合物中C2H8N2的质量为14g÷(
| 14×2 |
| 12×2+1×8+14×2 |
| 1×8 |
| 12×3 |
故答案为:(1)3:1;(2)40;(3)56g;(4)1:1;(5)6g.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
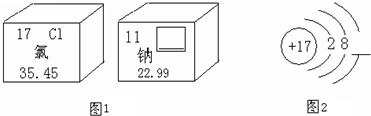 26、图1是两种元素在元素周期表中的信息,图2是氯原子的原子结构示意图
26、图1是两种元素在元素周期表中的信息,图2是氯原子的原子结构示意图