题目内容
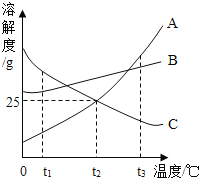
【题目】(5分)根据A物质和B物质的溶解度曲线(如图), 回答下列问题:

(1)10℃时,A、B两种物质的溶解度大小关系
是A B(填“>”、“<”或“=”)
(2)40℃时,将40g B物质放人100g水中,形成的溶液是 溶液(填“饱和”或“不饱和”),此时溶质质量分数是 。(精确到0.1%);现将该溶液降温至20℃,析出固体 g。
(3)已知NaCl的溶解度如下表,请在上图中描出NaCl的溶解度曲线。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
【答案】(1) < ;(2)不饱和, 28.6% ; 0 ;(3)略 (1分 ,连成圆滑的曲线可得分,曲线上未标注物质不作扣分点)
【解析】
试题分析:依据曲线可得:(1)10℃时,A、B两种物质的溶解度大小关系是A<B;(2)40℃时,B的溶解度为50g>40g 形成不饱和溶液,其溶质为40g,溶剂为100g,溶液为140g,依据溶质质量分数的计算公式即可得出;降温至20℃时,其溶解度为40g,正好饱和,没有固体析出。

 期末集结号系列答案
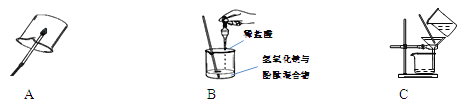
期末集结号系列答案【题目】(8分)在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的研究。
探究一: M溶液中的溶质是什么?
【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是_____________,②是CaCl2
【收集资料】碳酸钠溶液与中性的CaCl2溶液能发生复分解反应。
【设计实验】同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴加___________ | ___________ | 猜想①正确 |
探究二:过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:____________;猜想三:NaOH
【实验验证】同学们针对“猜想一”进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | “猜想一”不成立 |
他们的实验结论是否正确?_________________,理由是_________________。
【继续探究】设计实验方案确定滤液中溶质的组成.
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入Na2CO3溶液 | __________________ __________________ | “猜想一”成立 |
【反思拓展】:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑_____。