题目内容
【题目】初中化学常见物质 A--G有如下图所示的转化关系(部分反应条件及物质己略去)。已知A为单质: C为气体,反应②为实验室制取气体C的方法, E是目前年产量最高的金属,F燃烧产生蓝色火焰。
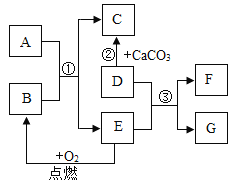
(1)反应①的基本反应类型为_____;
(2)写出物质的名称:C: _____;
(3)写出反应③的现象: _____;
(4)写出有关反应的化学方程式:
E在氧气中燃烧: _____;反应①: _____;反应③: _____。
(5) 23.2 g某种E的氧化物与一氧化碳充分反应生成16.8g的E和17.6 g的二氧化碳,若用碳单质将等质量的该氧化物还原成E,则生成二氧化碳的质量为_____ g。
【答案】置换反应 二氧化碳 固体表面有气泡产生,溶液由无色变为浅绿色 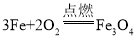 2C+Fe3O4
2C+Fe3O4![]() 3Fe +2CO2↑
3Fe +2CO2↑ ![]() 8.8
8.8
【解析】
反应②为实验室制取气体C的方法,反应物之一是碳酸钙,则C是二氧化碳,D是稀盐酸;E是目前年产量最高的金属,E是铁,铁与稀盐酸反应生成氯化亚铁和氢气,F燃烧产生蓝色火焰,F是氢气。铁在氧气中燃烧生成四氧化三铁,B是四氧化三铁,四氧化三铁与A反应生成二氧化碳和铁,A是单质,则A是碳。将推出的各种物质代入转化关系中进行验,推断正确。
(1)反应①是:2C+Fe3O4![]() 3Fe +2CO2↑,由一种单质与一种化合物反应生成另一种单质与另一种化合物的反应是置换反应,该反应属于置换反应。
3Fe +2CO2↑,由一种单质与一种化合物反应生成另一种单质与另一种化合物的反应是置换反应,该反应属于置换反应。
(2)由分析可知,C是二氧化碳。
(3)反应③是铁与稀盐酸的反应,会观察到固体表面有气泡产生,溶液由无色变为浅绿色。
(4)E在氧气中燃烧的化学方程式为: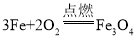 ;反应①为:2C+Fe3O4
;反应①为:2C+Fe3O4![]() 3Fe +2CO2↑;反应③为:
3Fe +2CO2↑;反应③为:![]() 。
。
(5) 设该氧化物的化学式为FexOy,则
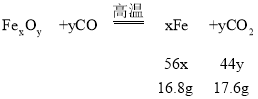
![]() ,解得:
,解得:![]() ,故该氧化物为Fe3O4。
,故该氧化物为Fe3O4。
Fe3O4+4CO![]() 3Fe+4CO2,Fe3O4+2C
3Fe+4CO2,Fe3O4+2C![]() 3Fe +2CO2↑,由上面的两个化学方程式可知,当用碳单质还原金属氧化物时,生成二氧化碳的质量是原来的
3Fe +2CO2↑,由上面的两个化学方程式可知,当用碳单质还原金属氧化物时,生成二氧化碳的质量是原来的![]() ,故若用碳单质将等质量的该氧化物还原成E,则生成二氧化碳的质量为8.8g。
,故若用碳单质将等质量的该氧化物还原成E,则生成二氧化碳的质量为8.8g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案