题目内容
(6分)根据表中内容回答下列问题。
|
|
0 |
20 |
40 |
60 |
80 |
||||||||||||||||||
|
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
||||||||||||||||||
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
||||||||||||||||||
|
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.116 |
0.094 |
(1)随温度升高,硝酸钾溶解度的变化趋势是___ ____(填“增大”“减小”或“不变”)。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是 ___ ____。
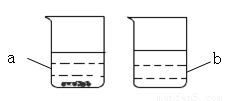
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100 g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质___ ____。
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是___ ____。
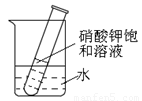
(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是___ ____。
(1)增大。
(2)大于20℃小于40℃。
(3)NaCl。
(4)烧杯内水温下降,试管中有晶体析出;
(5)烧杯内浑浊,水温上升,试管内固体逐渐溶解。
【解析】
试题分析:(1)根据表格中的数据分析,硝酸钾的溶解度随温度的升高而升高。
(2)要判断硝酸钾与氯化钠溶解度相等时的温度范围,即判断该温度范围内两种物质的溶解度的数值是否存在相等的可能,经分析知在20~40℃时,这两种物质存在溶解度相同的可能。
(3)由表格数据可知,20℃时100g水中最多可溶解硝酸钾31.6g,可溶解氯化钠36g,所以,20℃时向100g水中分别加入36g溶质,氯化钠恰好全部溶解得到饱和溶液,而硝酸钾不会全部溶解,即有溶质剩余,故烧杯b中溶解的物质是氯化钠。
(4)硝酸铵溶解时吸收热量,会使温度降低;而由于硝酸钾的溶解度随温度的降低溶解度减小,故可观察到随烧杯内水温的下降,试管中的饱和的硝酸钾溶液会有晶体析出。
(5)生石灰与水反应,生成熟石灰的同时,会放出大量的热,使温度升高;由于熟石灰微溶于水,且随温度升高而溶解度变小,故可观察到烧杯内会变浑浊;而由于硝酸钾的溶解度随温度的升高溶解度增大,故随水温上的上升,试管内的固体会逐渐溶解。
考点:固体溶解度的影响因素,溶解时的吸热或放热现象
点评:解答这类题目时,要熟记和理解固体溶解度的影响因素及其随温度变化的规律,以及物质的溶解和结晶等相关知识;然后结合所学的相关知识和技能,按照题目的要求,认真地进行解答即可。

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案




 (5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是
(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是
 采取的方法有
采取的方法有 象,烧杯b中溶解的物质是
象,烧杯b中溶解的物质是