题目内容
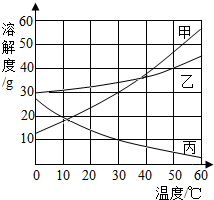
如图所示是甲、乙、丙三种固体物质的溶解度曲线,根据图示回答下列问题:
(1)30℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是______;
(2)当甲中混有少量的乙时,可采用______结晶的方法提纯甲;
(3)30℃时,将10g甲物质加入到盛有50g水的烧杯中,充分溶解后,所得溶液是甲物质的______(填“饱和”或“不饱和”)溶液;
(4)50℃时,分别配制甲、乙、丙三种物质的饱和溶液各100g,所需水的质量最少的是______(填“甲”、“乙”或“丙”);
(5)20℃时,配制一定量丙物质的溶液,将溶液升温到40℃时,是否有固体析出?______(填“有”、“没有”或“不确定”).
解:
(1)从30℃向上做垂线,与曲线的交点在上面的溶解度就大,所以30℃时它们的溶解度大小顺序是乙>甲>丙;
故答案为:乙>甲>丙(或乙、甲、丙);
(2)由图可知:甲的溶解度随温度变化较大,乙的溶解度受温度影响较小,故当甲中混有少量的乙时,可采用降温结晶(或冷却热饱和溶液)的方法提纯甲;
故答案为:降温(或冷却热饱和溶液);
(3)30℃时甲的溶解度是30g,所以50g水中最多溶解15g的甲;因此将10g甲物质加入到50g水充分溶解后,所得溶液是不饱和溶液;
故答案为:不饱和;
(4)50℃时,甲、乙、丙三种物质的溶解度从大到小是甲>乙>丙,即相等的水中溶解三种物质的大小顺序是甲>乙>丙;所以分别配制甲、乙、丙三种物质的饱和溶液各100g,所需溶质质量最多的是甲,需要水的质量最少;
故答案为:甲;
(5)虽然丙的溶解度曲线随温度升高而减小,但20℃时配制的一定量丙物质的溶液,不知溶液是否饱和,所以将溶液升温到40℃时,不确定是否有溶质析出;
故答案为:不确定.
分析:(1)根据某一温度时物质溶解度的比较方法分析解答;
(2)根据甲、乙溶解度曲线随温度变化情况分析解答;
(3)根据30℃时甲的溶解度分析解答;
(4)根据50℃时,甲、乙、丙三种物质的溶解度分析解答;
(5)根据题意并结合丙的溶解度曲线随温度变化情况分析解答.
点评:解答本题的关键是要明确溶解度的概念及对溶解度曲线的理解和应用,掌握相关知识才能正确解答,要细心逐一分析.
(1)从30℃向上做垂线,与曲线的交点在上面的溶解度就大,所以30℃时它们的溶解度大小顺序是乙>甲>丙;
故答案为:乙>甲>丙(或乙、甲、丙);
(2)由图可知:甲的溶解度随温度变化较大,乙的溶解度受温度影响较小,故当甲中混有少量的乙时,可采用降温结晶(或冷却热饱和溶液)的方法提纯甲;
故答案为:降温(或冷却热饱和溶液);
(3)30℃时甲的溶解度是30g,所以50g水中最多溶解15g的甲;因此将10g甲物质加入到50g水充分溶解后,所得溶液是不饱和溶液;
故答案为:不饱和;
(4)50℃时,甲、乙、丙三种物质的溶解度从大到小是甲>乙>丙,即相等的水中溶解三种物质的大小顺序是甲>乙>丙;所以分别配制甲、乙、丙三种物质的饱和溶液各100g,所需溶质质量最多的是甲,需要水的质量最少;
故答案为:甲;
(5)虽然丙的溶解度曲线随温度升高而减小,但20℃时配制的一定量丙物质的溶液,不知溶液是否饱和,所以将溶液升温到40℃时,不确定是否有溶质析出;
故答案为:不确定.
分析:(1)根据某一温度时物质溶解度的比较方法分析解答;
(2)根据甲、乙溶解度曲线随温度变化情况分析解答;
(3)根据30℃时甲的溶解度分析解答;
(4)根据50℃时,甲、乙、丙三种物质的溶解度分析解答;
(5)根据题意并结合丙的溶解度曲线随温度变化情况分析解答.
点评:解答本题的关键是要明确溶解度的概念及对溶解度曲线的理解和应用,掌握相关知识才能正确解答,要细心逐一分析.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
 26、如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
26、如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: 20、如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
20、如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:

 (2013?文昌一模)如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
(2013?文昌一模)如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: