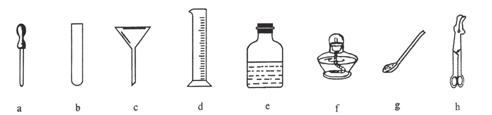
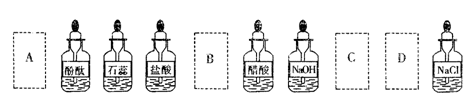
题目内容
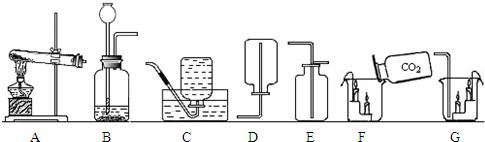
根据下图实验装置,回答有关问题:
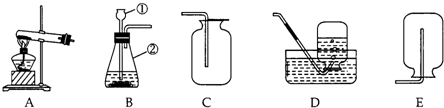
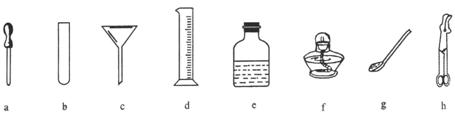
(1)在上图中写出标数字的仪器名称:①
(2)用双氧水和二氧化锰制取氧气的反应表达式为
(3)用排水法收集氧气时发现得到的氧气不纯,试分析其中的可能原因:
(4)大理石和稀盐酸制取二氧化碳的表达式为 图中的装置B.老师听取了两位同学的意见后,指出两套装置都可以作为制取二氧化碳的发生装置,但用装置B有一定的优点.请你思考后回答,装置B的优点是:
图中的装置B.老师听取了两位同学的意见后,指出两套装置都可以作为制取二氧化碳的发生装置,但用装置B有一定的优点.请你思考后回答,装置B的优点是:
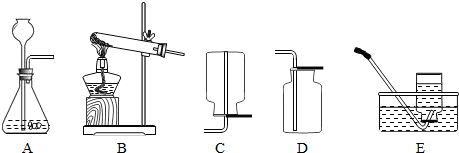
(5)通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水.实验室用加热氯化铵固体和消石灰固体的混合物来制取氨气.实验室制取和收集氨气的装置组合是

(1)在上图中写出标数字的仪器名称:①
长颈漏斗
长颈漏斗
,②锥形瓶
锥形瓶
;(2)用双氧水和二氧化锰制取氧气的反应表达式为
双氧水
水+氧气
| MnO2 |
双氧水
水+氧气
.| MnO2 |
(3)用排水法收集氧气时发现得到的氧气不纯,试分析其中的可能原因:
收集好氧气的集气瓶没有盖好玻璃片
收集好氧气的集气瓶没有盖好玻璃片
、没待气泡连续冒出就进行收集
没待气泡连续冒出就进行收集
、实验开始时集气瓶中没有灌满水
实验开始时集气瓶中没有灌满水
(说出三点).(4)大理石和稀盐酸制取二氧化碳的表达式为
碳酸钙+稀盐酸→氯化钙+水+二氧化碳
碳酸钙+稀盐酸→氯化钙+水+二氧化碳
.小明和小亮两位同学讨论选择制取二氧化碳的发生装置时,小明认为应选择右图中的装置A,小亮却认为应选择下 图中的装置B.老师听取了两位同学的意见后,指出两套装置都可以作为制取二氧化碳的发生装置,但用装置B有一定的优点.请你思考后回答,装置B的优点是:
图中的装置B.老师听取了两位同学的意见后,指出两套装置都可以作为制取二氧化碳的发生装置,但用装置B有一定的优点.请你思考后回答,装置B的优点是:随时控制反应的进行
随时控制反应的进行
、节约药品
节约药品
.(至少说出两点)(5)通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水.实验室用加热氯化铵固体和消石灰固体的混合物来制取氨气.实验室制取和收集氨气的装置组合是
A、E
A、E
;实验室制取氨气时,为防止多余的氨气逸散到空气中,可用水
水
吸收多余的氨气.分析:(1)依据对常见仪器的认识解决.
(2)根据实验室用双氧水制取氧气的实际情况分析解决.
(3)根据收集气体的注意事项考虑.
(4)从长颈漏斗及分液漏斗的不同分析优缺点.
(5)利用装置选择的标准结合氨气的性质分析并判断.
(2)根据实验室用双氧水制取氧气的实际情况分析解决.
(3)根据收集气体的注意事项考虑.
(4)从长颈漏斗及分液漏斗的不同分析优缺点.
(5)利用装置选择的标准结合氨气的性质分析并判断.
解答:解:(1)依据常见仪器的认识可知该仪器是长颈漏斗;锥形瓶.
(2)双氧水分解时一般二氧化锰作催化剂,生成水与氧气.
(3)收集的氧气不纯,可能是收集好氧气的集气瓶没有盖好玻璃片,或没待气泡连续冒出就进行收集或实验时集气瓶中没有灌满水等.
(4)选择装置B、A都可以用来制取二氧化碳,比较这两个装置的不同,B装置一个突出优点可以随时控制反应的进行且节约药品,减少酸的用量,发生的反应是:碳酸钙+稀盐酸→氯化钙+水+二氧化碳
(5)氨气是一种密度比空气小,极易溶于水的气体,所以只能用向下排气法收集;实验室用加热氯化氨和消石灰的固体混合物制取氨气,所以用A装置制取.氨气极易溶于水,所以可用水吸收多余的氨气.
故答案为:(1)长颈漏斗;锥形瓶(2)双氧水
水+氧气(3)收集好氧气的集气瓶没有盖好玻璃片;没待气泡连续冒出就进行收集;实验开始时集气瓶中没有灌满水(4)碳酸钙+稀盐酸→氯化钙+水+二氧化碳;随时控制反应的进行;节约药品
(5)AE;水
(2)双氧水分解时一般二氧化锰作催化剂,生成水与氧气.
(3)收集的氧气不纯,可能是收集好氧气的集气瓶没有盖好玻璃片,或没待气泡连续冒出就进行收集或实验时集气瓶中没有灌满水等.
(4)选择装置B、A都可以用来制取二氧化碳,比较这两个装置的不同,B装置一个突出优点可以随时控制反应的进行且节约药品,减少酸的用量,发生的反应是:碳酸钙+稀盐酸→氯化钙+水+二氧化碳
(5)氨气是一种密度比空气小,极易溶于水的气体,所以只能用向下排气法收集;实验室用加热氯化氨和消石灰的固体混合物制取氨气,所以用A装置制取.氨气极易溶于水,所以可用水吸收多余的氨气.
故答案为:(1)长颈漏斗;锥形瓶(2)双氧水
| MnO2 |
(5)AE;水
点评:本考点主要考查实验室中制取气体的装置和收集装置的选择,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

练习册系列答案
相关题目
 :
: