题目内容
(10陕西20)(化学方程式2分,其余每空l分,共5分)构建知识网络,可以帮助我们理解知识间的内在联系。如图是盐酸与不同类别物质之间反应的知识网络。
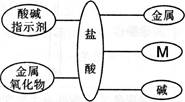
(1)图中M应为 类物质。
(2)写出一种能与盐酸反应的金属 。
(3)盐酸能与碱反应的实质是盐酸中的 (写离子符号)与碱中的0H?反应生成H2O。
(4)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 。

(1)图中M应为 类物质。
(2)写出一种能与盐酸反应的金属 。
(3)盐酸能与碱反应的实质是盐酸中的 (写离子符号)与碱中的0H?反应生成H2O。
(4)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 。
(1) 盐 (2) Zn或锌(其他合理答案均可) (3) H+
(4) Fe2O3+6HCl==2FeCl3+3H2O(未配平扣l分,化学式错误扣2分)
(4) Fe2O3+6HCl==2FeCl3+3H2O(未配平扣l分,化学式错误扣2分)
本题考查的是酸碱盐的应用,酸的化学性质,中和反应及其应用,书写化学方程式。把盐酸的性质用网络框架的形式表示出来,可以更直观的让学生了解和记忆,根据盐酸的化学性质分析:(1)跟指示剂反应; (2)跟活泼金属起置换反应;(3) 跟碱性氧化物反应;(4)跟某些盐反应;(5)跟碱起中和反应。
(1)盐酸可与五类物质发生化学反应,图中M应为其中的盐类物质。
(2)在金属活动性顺序中排在氢前面的金属都能和盐酸反应,常用的有铝、镁、锌、铁。
(3)酸碱中和的实质就是H++OH-→H2O。
(4)铁锈属于金属氧化物,与盐酸反应生成盐和水故化学方程式Fe2O3+6HCl==2FeCl3+3H2O
(1)盐酸可与五类物质发生化学反应,图中M应为其中的盐类物质。
(2)在金属活动性顺序中排在氢前面的金属都能和盐酸反应,常用的有铝、镁、锌、铁。
(3)酸碱中和的实质就是H++OH-→H2O。
(4)铁锈属于金属氧化物,与盐酸反应生成盐和水故化学方程式Fe2O3+6HCl==2FeCl3+3H2O

练习册系列答案
相关题目