题目内容
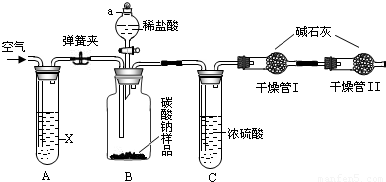
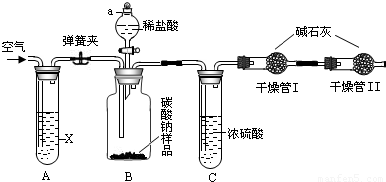
32、用含有少量生石灰的NaCl固体,配制一定质量分数的NaCl溶液.实验步骤如下图所示:
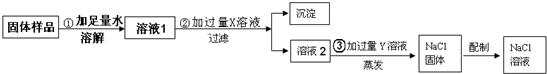
(1)溶液1中所含溶质为
(2)加入X发生反应的化学方程式为
(3)加入的Y为

(1)溶液1中所含溶质为
Ca(OH)2和NaCl
(填化学式).(2)加入X发生反应的化学方程式为
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
.(3)加入的Y为
HCl
(填化学式),所发生反应的化学方程式为Na2CO3+2HCI═2NaCl+H2O+CO2↑和NaOH+HCl═NaCl+H2O
.分析:(1)氧化钙与水反应生成氢氧化钙,氢氧化钙微溶于水,氯化钠能溶于水;
(2)加入过量X溶液的目的是除去溶液1中的氢氧化钙,结合后面的操作,可判断X溶液是碳酸钠溶液,根据反应物和生成物书写化学方程式,注意沉淀符合和配平;
(3)加入Y溶液的目的是为了除去Na2CO3和NaOH,同时不引进新的杂质,故Y是盐酸,根据反应物和生成物写出化学方程式.
(2)加入过量X溶液的目的是除去溶液1中的氢氧化钙,结合后面的操作,可判断X溶液是碳酸钠溶液,根据反应物和生成物书写化学方程式,注意沉淀符合和配平;
(3)加入Y溶液的目的是为了除去Na2CO3和NaOH,同时不引进新的杂质,故Y是盐酸,根据反应物和生成物写出化学方程式.
解答:解:(1)CaO与水反应的产物是Ca(OH)2,所以溶液A包括Ca(OH)2和NaCl,
(2)要除去氯化钠中的氢氧化钙,且能把带入的杂质按照后面的操作除去,那么X应该是碳酸钠溶液,它与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)加入过量Y溶液的目的是为了除去Na2CO3和NaOH,同时不引进新的杂质,那么Y应该是稀盐酸,它和氢氧化钠、碳酸钠反应都生成氯化钠,过量的盐酸可以通过蒸发的方法除掉.反应的化学方程式为:Na2CO3+2HCI═2NaCl+H2O+CO2↑;NaOH+HCl═NaCl+H2O
故答案为:(1)Ca(OH)2和NaCl
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
(3)HCl
Na2CO3+2HCI═2NaCl+H2O+CO2↑和NaOH+HCl═NaCl+H2O(答完整得1分)
(2)要除去氯化钠中的氢氧化钙,且能把带入的杂质按照后面的操作除去,那么X应该是碳酸钠溶液,它与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)加入过量Y溶液的目的是为了除去Na2CO3和NaOH,同时不引进新的杂质,那么Y应该是稀盐酸,它和氢氧化钠、碳酸钠反应都生成氯化钠,过量的盐酸可以通过蒸发的方法除掉.反应的化学方程式为:Na2CO3+2HCI═2NaCl+H2O+CO2↑;NaOH+HCl═NaCl+H2O
故答案为:(1)Ca(OH)2和NaCl
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
(3)HCl
Na2CO3+2HCI═2NaCl+H2O+CO2↑和NaOH+HCl═NaCl+H2O(答完整得1分)
点评:完成此类推断除杂题时,要根据物质的性质和每一步的实验目的,选择适当的除杂剂,书写化学方程式时一定要按照步骤进行,正确书写反应物和生成物的化学式,配平并注明反应条件.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目