题目内容
“用微观的眼光看世界”是学习化学的重要方法.按要求填空.
(1)用符号和数字填空
①3个氧气分子
Cl3
Cl3.
(2)日本的核泄漏使国人关注起食盐,食盐的主要成分NaCl由
2NaOH+H2↑+X↑,则X的化学式为
(3)已知硒的核电荷数为34,相对原子质量为79,由以上信息你还能得出关于该微粒的其它哪些结论
(1)用符号和数字填空
①3个氧气分子
3O2
3O2
;②2个氢氧根离子2OH-
2OH-
;③氯化铁中铁元素的化合价| +3 |
| Fe |
| +3 |
| Fe |
(2)日本的核泄漏使国人关注起食盐,食盐的主要成分NaCl由
离子
离子
(填“分子”、“原子”或“离子”)构成;通过晾晒海水等方法,可得到含有较多杂质的粗盐,这种方法属于物理
物理
变化(填“物理”或“化学”).除去食盐水中泥沙等不溶性杂质的方法是过滤
过滤
,电解食盐水发生反应的化学方程式为:2NaCl+2H2O
| ||
Cl2
Cl2
.(3)已知硒的核电荷数为34,相对原子质量为79,由以上信息你还能得出关于该微粒的其它哪些结论
硒原子原子核内质子数为34;硒原子的核外电子数为34;硒原子核内中子数为45等
硒原子原子核内质子数为34;硒原子的核外电子数为34;硒原子核内中子数为45等
.(至少写两点)分析:(1)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,进行书写;根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,进行书写.根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,进行书写.
(2)氯化钠是由氯离子和钠离子构成的离子化合物;根据化学变化和物理变化的本质区别进行分析判断;过滤可以除去不溶于水的物质;由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(3)根据原子中:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,进行分析解答.
(2)氯化钠是由氯离子和钠离子构成的离子化合物;根据化学变化和物理变化的本质区别进行分析判断;过滤可以除去不溶于水的物质;由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(3)根据原子中:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,进行分析解答.
解答:解:(1)根据分子的表示方法:正确书写物质的化学式;如O2表示一个氧分子,3个氧气分子可表示为3O2;
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个氢氧根离子表示为:2OH-;
书写化学式时要根据元素的化合价书写,标化合价时要把化合价表中元素符号的正上方,且正负号在数字的前面.氯化铁中铁元素显+3价,氯元素显-1价,故氯化铁中铁元素的化合价可表示为
Cl3.
(2)氯化钠是由氯离子和钠离子构成的离子化合物;从海水中得到粗盐晶体没有新物质生成,属于物理变化;过滤可以除去不溶于水的物质,食盐溶于水,泥沙不溶于水,所以可利用过滤的方法除去泥沙.根据反应的化学方程式2NaCl+2H2O
2NaOH+H2↑+X↑,反应物中钠、氯、氢、氧原子个数分别为2、2、4、2,反应后的生成物中钠、氯、氢、氧原子个数分别为2、0、4、2,根据反应前后原子种类、数目不变,则每个X分子由2个氯原子构成,则物质X的化学式为Cl2.
(3)由题意:硒的核电荷数为34,相对原子质量为79,根据原子中:核电荷数=质子数=电子数,可知硒原子原子核内质子数为34,核外电子数为34;根据相对原子质量=质子数+中子数,可知中子数=79-34=45.
故答案为:
(1)3O2;2OH-;
Cl3;
(2)离子;物理;过滤;Cl2;
(3)硒原子原子核内质子数为34;硒原子的核外电子数为34;硒原子核内中子数为45等.
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个氢氧根离子表示为:2OH-;
书写化学式时要根据元素的化合价书写,标化合价时要把化合价表中元素符号的正上方,且正负号在数字的前面.氯化铁中铁元素显+3价,氯元素显-1价,故氯化铁中铁元素的化合价可表示为
| +3 |
| Fe |
(2)氯化钠是由氯离子和钠离子构成的离子化合物;从海水中得到粗盐晶体没有新物质生成,属于物理变化;过滤可以除去不溶于水的物质,食盐溶于水,泥沙不溶于水,所以可利用过滤的方法除去泥沙.根据反应的化学方程式2NaCl+2H2O
| ||
(3)由题意:硒的核电荷数为34,相对原子质量为79,根据原子中:核电荷数=质子数=电子数,可知硒原子原子核内质子数为34,核外电子数为34;根据相对原子质量=质子数+中子数,可知中子数=79-34=45.
故答案为:
(1)3O2;2OH-;
| +3 |
| Fe |
(2)离子;物理;过滤;Cl2;
(3)硒原子原子核内质子数为34;硒原子的核外电子数为34;硒原子核内中子数为45等.
点评:本题难度不大,但综合性较强,掌握对常见化学用语(元素符号、化学式、离子符号等)的书写、常见物质的构成、过滤原理的应用、原子守恒来确定物质的化学式的方法、原子中核电荷数=质子数=电子数、相对原子质量=质子数+中子数等是正确解答本题的关键.

练习册系列答案
相关题目
 表示
表示 ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示
”表示 表示
表示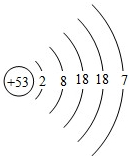 ,则碘元素在元素周期表中位于第
,则碘元素在元素周期表中位于第 ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示
”表示
 表示氧原 子,
表示氧原 子, 表示氢原子写出该反应的化学方程式:
表示氢原子写出该反应的化学方程式: