题目内容
23、科学研究表明:同一种元素的原子中其质子数都相同,但中子数却不一定相同.碳元素中就有三种这样的原子,质子数、中子数分别为6、6;6、7;6、8,分别记作为C-12、C-13、C-14原子.
(1)C-12与C-13的化学性质
(2)画出C-14的原子结构示意图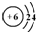 ;
;
(3)如果C-14与O原子结合成CO2,则这种CO2的相对分子质量是
(1)C-12与C-13的化学性质
相同
(填“相同”或“不相同”);(2)画出C-14的原子结构示意图
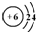
(3)如果C-14与O原子结合成CO2,则这种CO2的相对分子质量是
46
.分析:(1)元素的化学性质取决于最外层电子数.
(2)C-14具有6个质子6个电子.
(3)相对原子质量等于个元素原子量之和.
(2)C-14具有6个质子6个电子.
(3)相对原子质量等于个元素原子量之和.
解答:解:(1)元素的化学性质取决于最外层电子数,三种原子的质子数相同则电子数也一定相同,所以最外层电子数也相同.
(2)C-14具有6个质子6个电子,核外分为两个个电子层,第一层4个第二层2个.
(3)相对原子质量等于个元素原子量之和,已知质子数加中子数与等于原子量,所以C-14的原子量=6+8=14,因此该二氧化碳的相对分子质量=14+16×2=46.
故答案为:
(1)相同;
(2)如图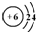 ;
;
(3)46.
(2)C-14具有6个质子6个电子,核外分为两个个电子层,第一层4个第二层2个.
(3)相对原子质量等于个元素原子量之和,已知质子数加中子数与等于原子量,所以C-14的原子量=6+8=14,因此该二氧化碳的相对分子质量=14+16×2=46.
故答案为:
(1)相同;
(2)如图
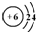 ;
;(3)46.
点评:此题是一道关于原子结构的考查题,解题的关键是掌握两个等式①原子中质子数=电子数②相对原子质量=质子数+中子数.

练习册系列答案
相关题目