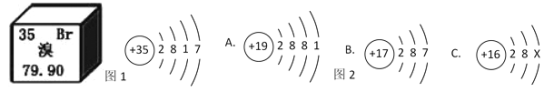
题目内容
【题目】因储存不当而发霉的粮食会产生黄曲霉素(化学式为 C17H12O6),人类使用会诱发癌症.下 列说法中正确的是( )
A. 黄曲霉素属于氧化物
B. 黄曲霉素由碳、氢、氧三种元素组成
C. 黄曲霉素中含有 17 个碳原子、12 个氢原子和 6 个氧原子
D. 黄曲霉素中碳、氢、氧三种元素的质量比为 17:12:6
【答案】B
【解析】
A、由两种元素组成的化合物,如果其中一种元素是氧,这样的化合物我们叫做氧化物,黄曲霉素是由碳、氢、氧三种元素组成的化合物,不属于氧化物,错误;B、黄曲霉素是由碳、氢、氧三种元素组成的化合物,正确;C、黄曲霉素是由分子构成的物质,每个黄曲霉素分子中含有17 个碳原子、12 个氢原子和 6 个氧原子,错误;D、黄曲霉素中碳、氢、氧三种原子的个数比为 17:12:6,而质量比是![]() ,错误。故选B。
,错误。故选B。

【题目】烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如下图,下列一定能正确反应X、Y对应关系的是( )
选项 | 烧杯内原有物质 | X | Y |
A | NaCl溶液 | NaCl固体 | NaCl溶液的溶质质量分数 |
B | 水 | NH4NO3固体 | 溶液的温度 |
C | 硫酸锌溶液 | 镁粉 | 溶液中溶质的质量 |
D | 稀硫酸 | 氧化镁 | 溶液中氧元素的质量 |
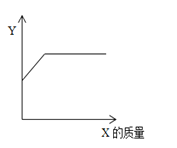
A. A B. B C. C D. D
【题目】实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水;
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分。
【猜想与假设】该黑色固体可能是①碳粉;② ;③碳和氧化铜的混合物。
【设计方案】请帮助该同学完成下述实验报告:
实验操作与现象 | 实验结论 |
猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O.
【进行实验】选择如下图所示装置进行验证:
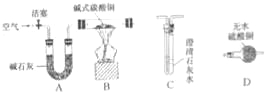
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→ → (填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到 ,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式 ;
②写出Cu2(OH)2CO3受热分解的化学方程式 。
【反思与评价】
上述装置中A的作用是 。
【题目】某课外兴趣小组为了测定当地石灰石中CaCO3的质量分数,取25g石灰石样品,粉碎后,将100g一定质量分数的稀盐酸分5次加入到该样品中,所测数据如下表所示(杂质不与稀盐酸反应,也不溶于水):
次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
产生气体的质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
(1)生成CO2的质量为_________g;
(2)第__________次恰好完全反应;
(3)求石灰石样品中CaCO3的质量分数。_________