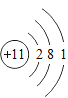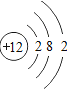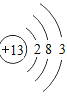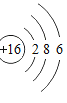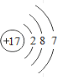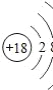题目内容
【题目】将 10g 质量分数为 10%的氯化钠溶液浓度变为 20%,下列操作正确的是( )
A.蒸发 5g 水B.加入氯化钠固体 1g
C.倒出一半溶液D.加入 10g 质量分数为 20%的氯化钠溶液
【答案】A
【解析】
10g 质量分数为10%的氯化钠溶液中氯化钠的质量为![]() ,溶剂的质量为
,溶剂的质量为![]() 。
。
A、设蒸发水的质量为 x,![]() ×100%=20%,x=5g,故A正确;
×100%=20%,x=5g,故A正确;
B、设加入氯化钠的质量为 y, ![]() ×100%=20%,y=1.25g,故B不正确;
×100%=20%,y=1.25g,故B不正确;
C、由于溶液的均一性,倒出一半溶液,溶液的浓度不变,故C不正确;
D、将 10g 质量分数为 10%的氯化钠溶液加入 10g 质量分数为 20%的氯化钠溶液, 溶液的浓度小于 20%,故D不正确。故选A。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】下表为元素周期表中某一周期元素的原子结构示意图.
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
请回答下列问题:
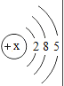
(1)表中磷原子的核电荷数x=____.
(2)表中具有相对稳定结构的元素是___.
(3)钠元素与氯元素形成的化合物化学式为span>___.
(4)上述元素在周期表中处于同一周期的原因是___.
(5)某元素的原子结构示意图如图所示,该元素符号为Br.
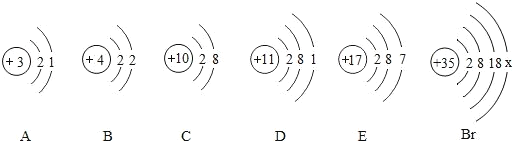
如图表示的微粒中,具有相对稳定结构的是___(填序号,下同),与 Br化学性质相似的是___.
【题目】今年扬州迎来高铁交通发展的高潮。高铁给我们带来的不仅是交通方便,出行快捷,甚至是带来旅游业的繁荣。制造铁轨需要大量的合金钢,梅岭中学化学兴趣小组为此展开探究:
(一)工业上炼铁炼钢和轧制钢材的主要流程如下图:
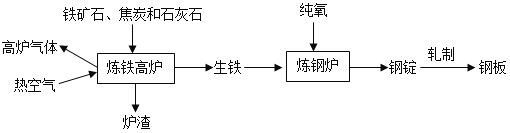
已知:生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)炼铁的固体原料中加入焦炭的作用是______________、___________(用方程式表示);
(2)炼铁的固体原料需经过粉碎,其目的是____________________ 。
(3)热空气和高炉气体的主要成分有一种相同,这种气体是________(填化学式);
(4)炼钢炉中,通入纯氧而不用空气的目的是____________________。将钢锭轧成钢板,体现了金属的________性。
(二)该兴趣小组发现未经处理的钢铁容易生锈。同学们接着探究了铁生锈的相关问题。
(知识回顾)铁生锈的条件为铁与_______、_______同时接触,为了防止铁制品生锈,应采取的措施是__________(写出一种)。
(查阅资料)铁锈成分复杂,化学式可简单表示为Fe2O3xH2O,在加热时会分步反应, 首先失去结晶水,其反应可表示为Fe2O3nH2O=Fe2O3+nH2O浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
(提出问题)铁锈(Fe2O3nH2O)中n的值等于多少呢?
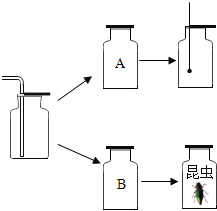
(问题探究)小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。
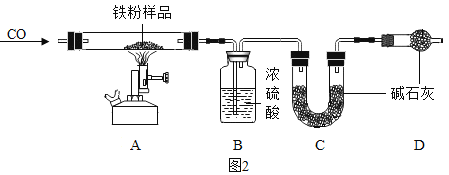
(1)实验前应先_______________;
(2)为了保证实验安全,实验开始时应先__________,目的是_______________;
(3)A中的现象是 ________________;
(4)请指出该装置中有一处明显不足 _____________;
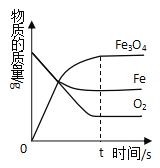
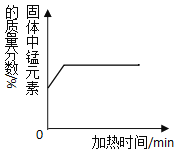
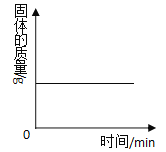
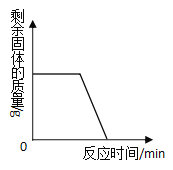
(数据处理)如图是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。
反应前(g) | 反应后(g) | |
B | 100 | 105.4 |
C | 150 | 163.2 |
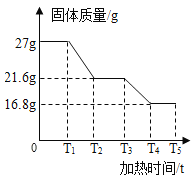
(5)铁锈(Fe2O3nH2O)中n的值是_____;
(6)写出T3-T4时间段发生反应的化学方程式 _______________________;
(7)计算原样品中单质铁的质量分数是________。(计算结果保留到0.1%)