题目内容
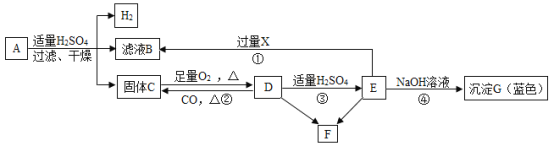
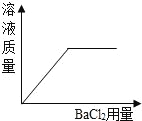
【题目】化学实验课上,某同学向含有稀硫酸的硫酸铜溶液中,逐滴滴入NaOH溶液至过量。记录滴入NaOH溶液质量(x)与有关量的变化关系如图所示(提示:硫酸铜溶液呈酸性),下列判断错误的是

A.图中纵坐标(y)表示生成Cu(OH) 2的质量
B.反应进行到B点时,溶液中的溶质是Na2SO4
C.AB段溶液的pH逐渐增大
D.B点和C点溶液的pH相等
【答案】D
【解析】
试题向含有稀硫酸的硫酸铜溶液中,逐滴滴入NaOH溶液至过量,加入的NaOH溶液是先和稀硫酸反应:2NaOH+H2SO4=Na2SO4+2H2O,再与硫酸铜溶液反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,所以图象中的OA段表示的就是发生了反应:2NaOH+H2SO4=Na2SO4+2H2O,,AB段表示的是发生了反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,A、图中纵坐标(y)表示生成Cu(OH) 2的质量,正确,B、反应进行到B点时,,两个反应都充分进行,第二个反应也是恰好反应,所以此时溶液中的溶质是Na2SO4,正确,C、AB段表示的是发生了反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,把呈弱酸性的CuSO4反应掉,生成了中性的Na2SO4,所以AB段溶液的pH逐渐增大,正确,D、BC段表示的是NaOH溶液过量,随着NaOH溶液加入,碱性应该逐渐增强,错误,故选D

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】常温下,往盛有一定量液体甲的烧杯中逐渐加人固体乙并充分搅拌。如图所示中横坐标工表示固体乙的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是
甲 | 乙 | y | |
A | 稀盐酸 | 氧化铜 | 溶液的质量 |
B | 水 | 氢氧化钠 | 溶液的质量 |
C | 饱和石灰水 | 生石灰 | 溶质的质量 |
D | 硝酸银溶液 | 铜粉 | 溶质的质量 |

A.AB.BC.CD.D
【题目】为测定某赤铁矿中氧化铁的质量分数,化学小组同学将12.5 g赤铁矿粉加到烧杯中,并把100 g稀硫酸分四次加入其中(赤铁矿中的其它成分既不溶于水又不和稀硫酸发生反应),每次加入稀硫酸并充分反应后的相关数据如下表。请计算:
实验次数 | 一 | 二 | 三 | 四 |
加入稀硫酸质量/g | 20.0 | 20.0 | 20.0 | 20.0 |
剩余固体质量/g | 8.5 | 4.5 | 2.5 | 2.5 |
(1)实验所用赤铁矿中氧化铁的质量是__。
(2)实验所用稀硫酸中溶质的质量分数___。